题目内容
将百分比浓度为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是( )C
| A.c2=c1 | B.c2<2c1 |
| C.c2>2c1 | D.无法确定 |
C
解析试题分析:硫酸溶液的质量分数由a%变为2a%,说明蒸发掉的水的质量为原溶液质量的一半。设硫酸溶液的质量为m,则蒸发前溶液的体积V前= ,蒸发后溶液的体积V后=
,蒸发后溶液的体积V后=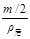 。因硫酸的密度随着溶液的浓度增大而变大,所以ρ前<ρ后,因此V前>2V后,c2>2c1。答案选C。
。因硫酸的密度随着溶液的浓度增大而变大,所以ρ前<ρ后,因此V前>2V后,c2>2c1。答案选C。
考点:物质的量浓度计算
点评:本题的关键就是硫酸的密度随着浓度的变化而改变,所以要考虑蒸发后密度的改变。

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
将百分比浓度为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是C
| A.c2=c1 | B.c2<2c1 | C.c2>2c1 | D.无法确定 |
将百分比浓度为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是( )C
| A.c2=c1 | B.c2<c1 | C.c2>2c1 | D.无法确定 |