��Ŀ����
��1-20��Ԫ���еļ������ĵ��Ӳ�ṹ��Ϊ ������������������д�������ݣ�
������������������д�������ݣ�
A��һ�㲻���������ʷ�����Ӧ����A���ĵ���ʽΪ ��
B����Ӧ��ԭ���У�L���������K���������3������B��Ϊ ��
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����CΪ ��B����C���γɵ�C2B�ĵ���ʽ�� ��
E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��ù����� ������ӻ�������ۻ��������������ʵ��֤���������ӻ����ﻹ�ǹ��ۻ����� ��
 ������������������д�������ݣ�
������������������д�������ݣ�A��һ�㲻���������ʷ�����Ӧ����A���ĵ���ʽΪ
B����Ӧ��ԭ���У�L���������K���������3������B��Ϊ
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����CΪ
E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��ù�����
���㣺ԭ�ӽṹ��Ԫ�ص�����
ר�⣺ԭ�������ṹר��
������A��һ�㲻���������ʷ�����Ӧ��ӦΪϡ������ԭ�ӣ���A��ΪNeԭ�ӣ�
B����Ӧ��ԭ���У�L���������K���������3������Bԭ��L�������Ϊ6��BΪOԪ�أ���B�������ӣ�
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����Cԭ�Ӻ��������=10+1=11����CΪ�����ӣ�B����C���γɵ�C2BΪNa2O�����������������ӹ��ɣ�
E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��E���Ӵ�2����λ����ɣ���Eԭ�Ӻ��������=10+2=12����E��Ϊþ���ӣ���ɫ����Ϊ������þ��
B����Ӧ��ԭ���У�L���������K���������3������Bԭ��L�������Ϊ6��BΪOԪ�أ���B�������ӣ�
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����Cԭ�Ӻ��������=10+1=11����CΪ�����ӣ�B����C���γɵ�C2BΪNa2O�����������������ӹ��ɣ�
E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��E���Ӵ�2����λ����ɣ���Eԭ�Ӻ��������=10+2=12����E��Ϊþ���ӣ���ɫ����Ϊ������þ��
���
�⣺A��һ�㲻���������ʷ�����Ӧ��ӦΪϡ������ԭ�ӣ���A��ΪNeԭ�ӣ�����ʽΪ��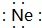 ��
��
B����Ӧ��ԭ���У�L���������K���������3������Bԭ��L�������Ϊ6��BΪOԪ�أ���B�������ӣ����ӷ���Ϊ��O2-��
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����Cԭ�Ӻ��������=10+1=11����CΪ�����ӣ����ӷ���ΪNa+��B����C���γɵ�C2BΪNa2O�����������������ӹ��ɣ�����ʽΪ��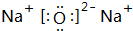 ��
��
E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��E���Ӵ�2����λ����ɣ���Eԭ�Ӻ��������=10+2=12����E��Ϊþ���ӣ���ɫ����Ϊ������þ���������ӻ��������ͨ���ⶨ����״̬�µ����ԣ�������˵�������ӻ���������ǹ��ۻ����
�ʴ�Ϊ��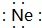 ��O2-��Na+��
��O2-��Na+��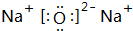 �����ӻ�����ⶨ����״̬�µ����ԣ�
�����ӻ�����ⶨ����״̬�µ����ԣ�
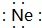 ��
��B����Ӧ��ԭ���У�L���������K���������3������Bԭ��L�������Ϊ6��BΪOԪ�أ���B�������ӣ����ӷ���Ϊ��O2-��
C�������Ժ����������һ�����Ӻ��γɵĵ����Ե�ԭ�ӻ�ԭ�Ժ�ǿ����Cԭ�Ӻ��������=10+1=11����CΪ�����ӣ����ӷ���ΪNa+��B����C���γɵ�C2BΪNa2O�����������������ӹ��ɣ�����ʽΪ��
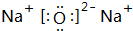 ��
��E��1mol����2mol OH -�γ�һ�ְ�ɫ���ܵĹ��壬��E���Ӵ�2����λ����ɣ���Eԭ�Ӻ��������=10+2=12����E��Ϊþ���ӣ���ɫ����Ϊ������þ���������ӻ��������ͨ���ⶨ����״̬�µ����ԣ�������˵�������ӻ���������ǹ��ۻ����
�ʴ�Ϊ��
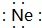 ��O2-��Na+��
��O2-��Na+��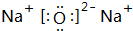 �����ӻ�����ⶨ����״̬�µ����ԣ�
�����ӻ�����ⶨ����״̬�µ����ԣ�
���������⿼��ԭ�ӽṹ��Ԫ�����ʣ��Ƚϻ�����ע���������ӻ������빲�ۻ��������ʱ�������

��ϰ��ϵ�д�
�����Ŀ
�������ӵĽṹʾ��ͼ�У���ʾ��ԭ�ӵ��ǣ�������
A�� |
B�� |
C�� |
D�� |
��һ���¶��£���һ���������ܱ������У���Ӧ2SO2��g��+O2��g��?2SO3��g���ﵽƽ��״̬�ı�־�ǣ�������
| A����λʱ��������n mol O2��ͬʱ����2n mol SO3 |
| B�������е���ѹǿ����ʱ��ı仯���ı� |
| C��������SO2��O2��SO3�����ʵ�����Ϊ2��1��2 |
| D�����������ܶȱ��ֲ��� |
NA��ʾ�����ӵ������������ж���ȷ���ǣ�������
| A��1mol�κ����������ķ�������ΪNA�� |
| B����״����22.4L��SO3�к���NA������ |
| C��1mol Cl2��������ˮ��һ��ת��NA������ |
| D��18g 18O2��18O3��һ������NA��18Oԭ�� |
���и���������ָ����Һ��һ���ܴ���������ǣ�������
| A��ˮ�����c��H+��=1��10-13mol/L����Һ�У�Na+��Ba2+��Cl-��NO3- |
| B��ʹ��̪���ɫ����Һ��Na+��Cu2+��HCO3-��NO3- |
| C�������������£�Fe2+��Cl-��NO3-��K+ |
| D������ɫ��Һ�У�Al3+��Cl-��K+��AlO2- |
