题目内容
2.关于SO2下列变化和其性质对应关系正确的是( )| A. | 品红溶液褪色---漂白性 | B. | 高锰酸钾溶液褪色---漂白性 | ||
| C. | 导致酸雨---酸性氧化物 | D. | 通入H2S溶液中变浑浊---氧化性 |
分析 SO2性质有:①具有酸性氧化物的通性;②具有还原性,被氧化剂氧化成SO3;③弱氧化性;④漂白性,能够和某些有色物质结合生成无色物质,但是不能漂白酸碱指示剂,以此解答该题,
A.二氧化硫具有选择漂白性
B.二氧化硫具有还原性和氧化性的高锰酸钾溶液发生氧化还原反应;
C.二氧化硫是硫酸型酸雨的形成原因;
D.二氧化硫中硫元素化合价处于+4价,具有弱氧化性,和硫化氢反应生成硫单质和水.
解答 解:A.SO2具有漂白性,能够和某些有色物质结合生成无色物质,但是不能漂白酸碱指示剂,能使品红溶液褪色,故A正确;
B.SO2具有还原性,被氧化剂氧化成SO3或者硫酸,故能使酸性KMnO4溶液褪色,故B错误;
C.SO2具有酸性氧化物的通性,空气中的二氧化硫能够和水反应生成亚硫酸,空气中氧化为硫酸,随雨水落下形成酸雨,二氧化硫是导致酸雨的原因,但酸性氧化物不一定形成酸雨,形成酸雨的物质是硫酸,故C错误;
D.二氧化硫中硫元素化合价处于+4价,具有弱氧化性,通入H2S溶液中变浑浊,反应为SO2+2H2S=3S+2H2O,二氧化硫表现的是氧化性,故D正确;
故选AD.
点评 本题考查二氧化硫的性质,为高频考点,侧重二氧化硫性质的考查,注重基础知识的夯实,注意相关物理性质的记忆,题目较简单.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
13.某溶液中大量存在以下五种离子NO3-、SO42-、Al3+、H+、M.其物质的量浓度之比为c(NO3-):c(SO42-):c(Al3+):c(H+):c(M)=4:3:1:3:2,则M可能是( )
| A. | Fe2+ | B. | Cl- | C. | Mg2+ | D. | Ba2+ |
17.由水电离出的c(OH-)=1×10-13 mol•L-1的无色溶液中,一定能大量共存的离子组是( )
| A. | Cl-、HCO3-、Na+、K+ | B. | NO3-、Ba2+、K+、Cl- | ||
| C. | Fe3+、NO3-、K+、H+ | D. | Al3+、SO42-、NH4+、Cl- |
7.下列物质既能与盐酸反应,又能与烧碱溶液反应的是( )
①Al2O3 ②SiO2 ③Al ④CaCO3 ⑤Fe(OH)3 ⑥NaHCO3 ⑦NaHSO4 ⑧Al(OH)3.
①Al2O3 ②SiO2 ③Al ④CaCO3 ⑤Fe(OH)3 ⑥NaHCO3 ⑦NaHSO4 ⑧Al(OH)3.
| A. | 除⑥外 | B. | 除⑤.⑥.⑦.⑧外 | C. | ①.②.⑥.⑦ | D. | ①.③.⑥.⑧ |
11.已知在1.01×105 Pa、298K条件下,2mol氢气燃烧生成液态水放出484kJ热量,下列表示氢气燃烧热的热化学方程式的是( )
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242 kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ•mol-1 | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ•mol-1 | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-242 kJ•mol-1 |
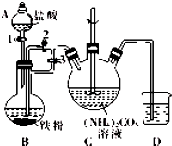 乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.
乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.