题目内容
实验室用乙酸和正丁醇制备乙酸正丁酯的原理如下:
CH3COOH+CH3CH2CH2CH2OH
CH3COOCH2CH2CH2CH3+H2O有关物质的物理性质如下表,请回答有关问题.
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸,然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及冷凝回流管,加热冷凝回流反应.
(1)沸石的作用 .
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是 ;
Ⅱ.乙酸正丁酯粗产品精制
(3)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠溶液洗涤.正确的操作步骤是 (填字母).
A.①②③④B.③①④②C.①④①③②D.④①③②③
CH3COOH+CH3CH2CH2CH2OH
| 浓硫酸 |
| 加热 |
| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/g |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸,然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及冷凝回流管,加热冷凝回流反应.
(1)沸石的作用
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是
Ⅱ.乙酸正丁酯粗产品精制
(3)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠溶液洗涤.正确的操作步骤是
A.①②③④B.③①④②C.①④①③②D.④①③②③
考点:乙酸乙酯的制取
专题:实验题
分析:(1)依据实验基本操作分析回答,沸石防暴沸;
(2)根据影响化学平衡移动的方法判断,减少生成物的量或增大另一种反应物的量都能使平衡向正反应方向移动;
(3)根据各物质的溶解性及性质进行排序.
(2)根据影响化学平衡移动的方法判断,减少生成物的量或增大另一种反应物的量都能使平衡向正反应方向移动;
(3)根据各物质的溶解性及性质进行排序.
解答:
解:Ⅰ.(1)在圆底烧瓶中加入沸石,防止加热时液体剧烈沸腾,物料喷出,故答案为:防止暴沸;
(2)实验中为了提高乙酸正丁酯的产率,使反应向正反应方向移动,所以采取的措施是用分水器及时移走反应生成的水,减少生成物的浓度;使用过量醋酸,提高正丁醇的转化率,
故答案为:用分水器及时移走反应生成的水,减小生成物的浓度,利用冷凝回流装置,提高反应物的转化率;
Ⅱ.(3)因为正丁醇和乙酸都具有挥发性,所以制取的酯中含有正丁醇和乙酸,第一步水洗除去酯中的正丁醇和乙酸;第二步用10%碳酸钠洗涤除去乙酸;
第三步用水洗涤除去碳酸钠溶液;第四步用无水硫酸镁干燥除去水;第五步蒸馏,制得较纯净的酯,
故选C.
(2)实验中为了提高乙酸正丁酯的产率,使反应向正反应方向移动,所以采取的措施是用分水器及时移走反应生成的水,减少生成物的浓度;使用过量醋酸,提高正丁醇的转化率,
故答案为:用分水器及时移走反应生成的水,减小生成物的浓度,利用冷凝回流装置,提高反应物的转化率;
Ⅱ.(3)因为正丁醇和乙酸都具有挥发性,所以制取的酯中含有正丁醇和乙酸,第一步水洗除去酯中的正丁醇和乙酸;第二步用10%碳酸钠洗涤除去乙酸;
第三步用水洗涤除去碳酸钠溶液;第四步用无水硫酸镁干燥除去水;第五步蒸馏,制得较纯净的酯,
故选C.
点评:本题考查了乙酸正丁酯的制取方法,侧重考查了灵活运用基础知识解决实际问题的能力,有利于培养学生的实验能力,和严禁的逻辑思维能力,注意实验化学来源于常规实验和基本操作的综合应用,题目难度不大.

练习册系列答案
相关题目
将1mol某饱和醇分成两等份.其中一份充分燃烧后生成1.5mol CO2,另一份与足量钠反应生成5.6L H2(标准状况).这种醇分子结构中除羟基外,还有两种不同的氢原子.则这种醇是( )
A、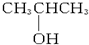 |
B、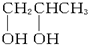 |
| C、CH3CH2CH2OH |
| D、CH3CH2OH |
下列叙述中能确定A金属性一定比B金属性强的是( )
| A、A原子的最外层电子数比B原子的最外层电子数少 |
| B、A原子的电子层数比B原子的电子层数多 |
| C、1 mol A与足量酸反应生成的H2比1 mol B与足量酸反应生成的H2多 |
| D、常温时,A能从水中置换出氢,而B不能 |
下列关于氧化物的叙述正确的是( )
①酸性氧化物肯定是非金属氧化物
②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物
④金属氧化物都是碱性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥不能跟酸反应的氧化物一定能跟碱反应.
①酸性氧化物肯定是非金属氧化物
②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物
④金属氧化物都是碱性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥不能跟酸反应的氧化物一定能跟碱反应.
| A、①②③④ | B、⑤⑥ |
| C、②③⑥ | D、③ |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到0.8g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A、至少存在5种离子 |
| B、Cl-一定存在,且c(Cl-)≥0.1mol/L |
| C、SO42-、NH4+一定存在,Cl-可能不存在 |
| D、CO32-、Al3+一定不存在,K+可能存在 |
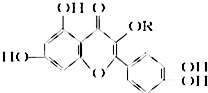 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、最多可以和含5 molBr2的溴水反应 |
| B、可用有机溶剂萃取 |
| C、分子中有三个苯环 |
| D、1 mol 维生素P可以和4 mol NaOH反应 |
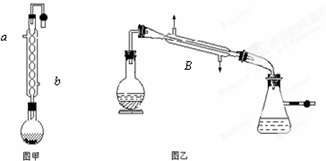
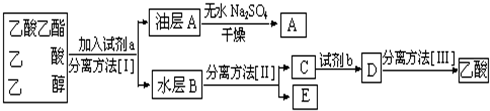
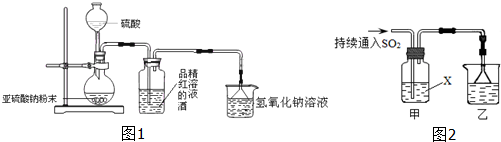
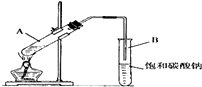 实验室用如图装置制取乙酸乙酯.
实验室用如图装置制取乙酸乙酯.