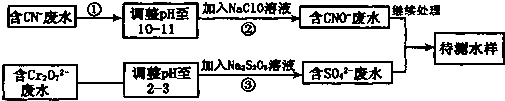
题目内容
同温同压下,下列有关等体积的二氧化碳和氢气的比较中,正确的是( )
| A、物质的量比为1:1 |
| B、密度比为11:1 |
| C、质量比为1:22 |
| D、质子数比为3:2 |
考点:阿伏加德罗定律及推论
专题:
分析:同温同压下,气体摩尔体积相等,相同体积的二氧化碳和氢气,根据n=
、ρ=
、m=nM、N=nNA结合分子构成计算.
| V |
| Vm |
| M |
| Vm |
解答:
解:同温同压下,气体摩尔体积相等,相同体积的二氧化碳和氢气,
A.根据n=
知,气体摩尔质量相等时,其体积之比等于物质的量之比,二者体积相等,所以其物质的量之比为1:1,故A正确;
B.根据ρ=
知,气体摩尔质量相等时,其密度之比等于摩尔质量之比=44g/mol:2g/mol=22:1,故B错误;
C.二者的物质的量相等,根据m=nM知,其质量之比等于摩尔质量之比=44g/mol:2g/mol=22:1,故C错误;
D.二者的物质的量相等,根据N=nNA知,二者的分子数相等,二氧化碳分子中质子数是22、氢气分子中质子数是2,所以其质子总数之比=22:2=11:1,故D错误;
故选A.
A.根据n=
| V |
| Vm |
B.根据ρ=
| M |
| Vm |
C.二者的物质的量相等,根据m=nM知,其质量之比等于摩尔质量之比=44g/mol:2g/mol=22:1,故C错误;
D.二者的物质的量相等,根据N=nNA知,二者的分子数相等,二氧化碳分子中质子数是22、氢气分子中质子数是2,所以其质子总数之比=22:2=11:1,故D错误;
故选A.
点评:本题考查阿伏伽德罗定律及其推论,侧重考查物质的量公式的运用,明确物质的量公式中各个物理量的关系是解本题关键,熟练掌握公式并灵活运用,题目难度不大.

练习册系列答案
相关题目
等质量的两份锌粉a、b分别加入到两份质量相同的过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,b保持不变,下列各图是产生H2的体积V(L)与时间t(min)的关系,其中正确的是( )
A、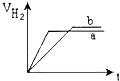 |
B、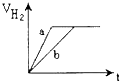 |
C、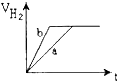 |
D、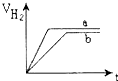 |
下列化学用语正确的是( )
| A、氟化氢的电子式:H:F |
| B、乙醇的分子式:CH3CH2OH |
C、硫原子的结构示意图: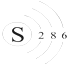 |
| D、Na2O2中即含有离子键,又含有非极性共价键 |
下列说法正确的是( )
| A、氨水能导电,所以氨气是电解质 |
| B、SO2的水溶液能导电,但是SO2是非电解质 |
| C、水溶液中NaHSO4=Na++HSO4- |
| D、FeCl3溶液为酸性,因为Fe3++3H2O=Fe(OH)3+3H+ |
想一想:NaOH、CuSO4、CH3COOH这些物质为什么可以归为一类,下列哪些物质还可以和它们归为一类( )
| A、CO2 |
| B、HCl(气态) |
| C、Fe(OH)3胶体 |
| D、NaOH溶液 |