题目内容
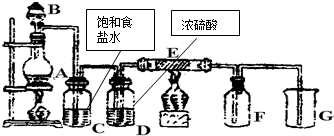 如图是实验室制取并收集Cl2的装置.A是Cl2发生装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置.
如图是实验室制取并收集Cl2的装置.A是Cl2发生装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置.试回答:(1)A中发生的化学反应方程式为
(2)C装置的作用是
(3)E中的反应方程式为
(4)写出G中反应的离子方程式
考点:氯气的实验室制法
专题:实验题
分析:(1)A装置是制取氯气的发生装置,二氧化锰与浓盐酸在加热条件制备氯气;
(2)浓盐酸具有挥发性,所以制备的氯气中含有氯化氢、水蒸气杂质,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,浓硫酸具有吸水性;
(3)氯气具有强的氧化性,铁丝在氯气中燃烧生成氯化铁;
(4)氯气有毒,直接排放能污染空气,氯气能够与氢氧化钠反应,被氢氧化钠吸收.
(2)浓盐酸具有挥发性,所以制备的氯气中含有氯化氢、水蒸气杂质,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,浓硫酸具有吸水性;
(3)氯气具有强的氧化性,铁丝在氯气中燃烧生成氯化铁;
(4)氯气有毒,直接排放能污染空气,氯气能够与氢氧化钠反应,被氢氧化钠吸收.
解答:
解:(1)A装置是制取氯气的发生装置,二氧化锰与浓盐酸在加热条件反应生成氯化锰、氯气和水,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)实验制备氯气中含杂质气体氯化氢和水蒸气,通入E装置时需要除去杂质,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,浓硫酸具有吸水性,所以通过盛有饱和食盐水C除去氯化氢,通过盛有浓硫酸的D除去水蒸气;
故答案为:除去氯气中的氯化氢气体;除去氯气中的水;
(3)铁丝在氯气中燃烧生成氯化铁,化学方程式为:2Fe+3Cl2
2FeCl3 ;
故答案为:2Fe+3Cl2
2FeCl3 ;
(4)氯气有毒需要用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
| ||
故答案为:MnO2+4HCl(浓)
| ||
(2)实验制备氯气中含杂质气体氯化氢和水蒸气,通入E装置时需要除去杂质,氯气在饱和食盐水中溶解度不大,氯化氢易溶于水,浓硫酸具有吸水性,所以通过盛有饱和食盐水C除去氯化氢,通过盛有浓硫酸的D除去水蒸气;
故答案为:除去氯气中的氯化氢气体;除去氯气中的水;
(3)铁丝在氯气中燃烧生成氯化铁,化学方程式为:2Fe+3Cl2
| ||
故答案为:2Fe+3Cl2
| ||
(4)氯气有毒需要用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
点评:本题考查了氯气的实验室制备原理、装置、杂质气体的处理、氯气性质的检验,明确氯气的性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
酸性H2CO3>HClO>HCO3-,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(Na+)>c(HCO3-)>c(H+)>c(OH-) |
| B、c(HCO3-)>c(ClO-)>c(OH-) |
| C、c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) |
| D、c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)+2c(CO32-) |
用物质的量均是0.1mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),下列对该混合溶液的判断正确的是( )
| A、c(H+)>c(OH-) |
| B、c(CH3COO-)+c(CH3COOH)=0.1 mol?L-1 |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(CH3COO-)+c(OH-)=0.1mol?L-1 |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
| A、K+、SiO32-、Cl-、NO3- |
| B、H+、NH4+、Al3+、SO42- |
| C、Na+、S2-、OH-、SO42- |
| D、Na+、C6H5O-、CH3COO-、HCO3- |
在某未知溶液中再溶入CH3COONa晶体,测得[Na+]与[CH3COO-]几乎相等,则原溶液可能是( )
| A、HCl溶液 |
| B、NaOH溶液 |
| C、KCl溶液 |
| D、KOH溶液 |
把镁条放入盛有过量盐酸的试管中,不影响氢气产生速率的是( )
| A、盐酸的浓度 |
| B、镁条的表面积 |
| C、加少量Na2SO4固体 |
| D、溶液的温度 |
下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
| A、CO2+H2O?H2CO3 | ||||
| B、3NO2+H2O═2HNO3+NO | ||||
C、3Fe+4H2O(g)
| ||||
| D、2Na+2H2O═2NaOH+H2↑ |
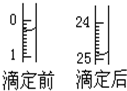 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.