题目内容
现有0.1mol/L的AlCl3溶液和0.1mol/L的氢氧化钠溶液,进行下面的实验。
(1)在试管中盛有上述AlCl3溶液10mL,向其中逐渐滴入上述的NaOH溶液。
①加入10mLNaOH溶液时的现象是_ ___,加入30mLNaOH溶液时的现象是_ ___,加入35mLNaOH溶液时的现象是_ ___。
②生成沉淀质量最多时,需NaOH溶液_ ___mL。
(2)向盛有10mLNaOH溶液的试管中滴入AlCl3溶液,同时不停摇动试管,出现的现象是_ ___,至加入多少毫升AlCl3溶液时开始出现沉淀?_ ___,至加入多少毫升AlCl3溶液时沉淀量最多?_ ___。写出上述过程的有关离子方程式_ ___。
(1)当NaOH溶液滴入10mL0.1mol/LAlCl3溶液中时,整个过程可用图象表示如下:
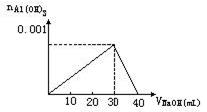
因为nAl3+=0.1×10×10-3=0.001(mol)
所以①当加入10mLNaOH溶液时现象是产生白色沉淀;加入30mL时,沉淀量最多;加入35mL时,沉淀部分溶解。
②生成沉淀最多时,需NaOH溶液30mL。
(2)当AlCl3溶液滴入NaOH溶液时,由于NaOH溶液是过量的,所以反应如下:
Al3++3OH-=Al(OH)3↓,
Al(OH)3+OH-=AlO2-+2H2O
上述两个方程式合并为:Al3++4OH-=AlO2-+2H2O,3AlO2-+Al3++6H2O=4Al(OH)3↓
可用图象表示如下:
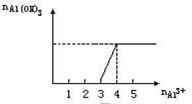 由于第一过程消耗的Al3+与第二过程消耗的Al3+之比为3:1,故开始产生沉淀与沉淀到最大所耗AlCl3溶液的体积比为3:1。
由于第一过程消耗的Al3+与第二过程消耗的Al3+之比为3:1,故开始产生沉淀与沉淀到最大所耗AlCl3溶液的体积比为3:1。
故开始时,现象为:有沉淀生成,但振荡后马上消失,开始沉淀时,需加入AlCl3的体积为xL
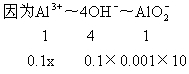
x=2.5(mL)
所以生成AlO2-为2.5×0.1×10-3mol=2.5×10-4mol
生成的AlO2-转化为Al(OH)3需Al3+为y
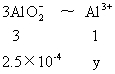
y=![]() (mol)
(mol)
沉淀最多时,需加入AlCl3的体积为![]()
![]() 0.1
0.1![]() 1000+2.5=
1000+2.5=![]() (mL)
(mL)

 阅读快车系列答案
阅读快车系列答案