题目内容
根据下列转化关系判断,下列说法正确的是
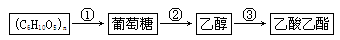
A.反应①中,(C6H10O5)n可表示淀粉或纤维素
B.反应②中,1 mol葡萄糖可生成3 mol乙醇
C.将在空气中灼烧后的铜丝趁热插入乙醇中主要得到乙酸
D.反应③得到的乙酸乙酯中含有乙醇和乙酸,可用饱和氢氧化钠溶液除去
A
【解析】
试题分析:A、高分子化合物水解得到葡萄糖的多糖是淀粉或纤维素,所以反应①中,(C6H10O5)n可表示淀粉或纤维素,正确;B、葡萄糖转化为乙醇的过程中还有二氧化碳生成,所以1mol的葡萄糖可生成2mol的乙醇,错误;C、乙醇在铜作催化剂、加热条件下与氧气的反应产物是乙醛,不是乙酸,错误;D、乙酸乙酯也与氢氧化钠溶液反应,所以不能用氢氧化钠除去乙酸乙酯中的乙醇和乙酸,应用饱和碳酸氢钠溶液,错误,答案选A。
考点:考查糖类、乙醇、乙酸乙酯的化学性质,

 小学教材完全解读系列答案
小学教材完全解读系列答案(9分)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)在酸性溶液中,水分子容易得到一个H+,形成水合氢离子(H3O+)。对于这一过程,下列描述不合理的是______________。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
根据价层电子对互斥理论推测H3O+的形状为_____________________。
(2)水分子和硫化氢分子的键角及中心原子的杂化方式如下表:
分子 | H2O | H2S |
中心原子杂化方式 | sp3 | |
键角 | 104.5° | 92.1° |
键长 | 95.7 pm | 133.6 pm |
根据表格中的数据判断O-H键键能______(填“>”、“=”或“<”)S-H键键能。用电负性知识解释H2O的键角大于H2S的键角的原因:________________________
__________________________________________________________。
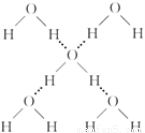
(3)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是________kJ/mol。