题目内容
在298K、1.01×105 Pa下,将22g CO2通入750mL 1mol/L NaOH溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1mol CO2通入1 L 2mol/L NaOH溶液中充分反应放出y kJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x)kJ/mol |
| B、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y)kJ/mol |
| C、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y)kJ/mol |
| D、CO2(g)+2NaOH(l)═2 NaHCO3(l)△H=-(8x-2y)kJ/mol |
考点:有关反应热的计算
专题:
分析:根据题意可知,22gCO2通入1mol?L-1NaOH溶液750mL中充分反应,测得反应放出xkJ的热量,写出热化学反应方程式,再利用1mol CO2通入2mol?L-1NaOH溶液1L中充分反应放出y kJ的热量写出热化学反应方程式,最后利用盖斯定律来书写CO2与NaOH溶液反应生成NaHCO3的热化学方程式.
解答:
解:根据题意,22gCO2通入1mol?L-1NaOH溶液750mL中充分反应,n(CO2)=0.5mol,n(NaOH)=1mol?L-1×0.75L=0.75mol,
该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO2+3NaOH═NaHCO3+Na2CO3+H2O,
由0.5molCO2反应放出热量为xkJ,则2molCO2反应放出热量为4xkJ,即热化学反应方程式为2CO2(g)+3NaOH(aq)═NaHCO3 (aq)+Na2CO3(aq)+H2O(l)△H=-4xkJ/mol①,
又1mol CO2通入2mol?L-1NaOH溶液1L中充分反应放出y kJ的热量,则热化学方程式为2NaOH(aq)+CO2(g)═Na2CO3(aq)+H2O(l)△H=-ykJ/mol②,
由盖斯定律可知,①-②可得,NaOH(aq)+CO2(g)═NaHCO3(aq)△H=-(4x-y)kJ/mol,
故选C.
该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO2+3NaOH═NaHCO3+Na2CO3+H2O,
由0.5molCO2反应放出热量为xkJ,则2molCO2反应放出热量为4xkJ,即热化学反应方程式为2CO2(g)+3NaOH(aq)═NaHCO3 (aq)+Na2CO3(aq)+H2O(l)△H=-4xkJ/mol①,
又1mol CO2通入2mol?L-1NaOH溶液1L中充分反应放出y kJ的热量,则热化学方程式为2NaOH(aq)+CO2(g)═Na2CO3(aq)+H2O(l)△H=-ykJ/mol②,
由盖斯定律可知,①-②可得,NaOH(aq)+CO2(g)═NaHCO3(aq)△H=-(4x-y)kJ/mol,
故选C.
点评:本题考查热化学方程式的书写和计算,是高考中常见题型,计算中涉及到化学方程式的有关计算问题和盖斯定律的有关应用,是一重点题型,学生还应注意在书写热化学方程式时标明各物质的状态.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关物质的性质和该性质的应用均正确的是( )
| A、浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 |
| B、二氧化硫有漂白性,可用于加工食品使食品增白 |
| C、铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| D、铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料 |
N2O俗称“笑气”,曾用作可吸入性麻醉剂.用以下反应可制取N2O:CO+NO2→CO2+N2O.下列说法正确的是( )
| A、反应中每生成1 mol N2O,消耗1.5 mol CO |
| B、等物质的量的N2O和CO2含有相等的电子数 |
| C、N2O只具有氧化性,无还原性 |
| D、反应中每生成1 mol N2O,电子转移的物质的量为3 mol |
以下物质是强电解质的是( )
| A、BaSO4 |
| B、浓H2SO4 |
| C、盐酸 |
| D、NH3 |
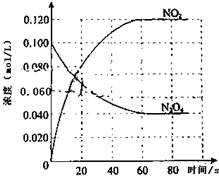 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题: