题目内容
19.体积相同、浓度均为0.2mol/L的盐酸和CH3COOH溶液,分别加水稀释m倍、n倍,溶液的pH都变成3,则m与n的关系为m>n.分析 醋酸为弱电解质,不能完全电离,若稀释后溶液pH相等,则盐酸稀释体积大于醋酸.
解答 解:醋酸为弱电解质,不能完全电离,若浓度均为0.2mol•L-1、等体积的盐酸和CH3COOH溶液分别加水稀释m倍、n倍,溶液的pH相同,即溶液中氢离子浓度相等,则盐酸稀释的倍数大于醋酸,即m>n;
故答案为:m>n.
点评 本题考查了强弱电解质在稀释时的离子浓度变化,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力,注意弱电解质的电离平衡.

练习册系列答案
相关题目
11.已知2H2(g)+O2(g)=2H2O(l)+571.6KJ.下列说法错误的是( )
| A. | 2mol液态水完全分解成氢气与氧气,需吸收571.6KJ热量 | |
| B. | 2mol氢气与1mol氧气的总能量大于2mol 液态水的总能量 | |
| C. | 2 g 氢气与16 g氧气完全反应生成18g液态水放出285.8 KJ热量 | |
| D. | 2mol氢气与1mol氧气完全反应生成水蒸汽放出的热量大于571.6KJ |
10.我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,如图所示为海水综合利用部分流程,有关说法正确的是( )
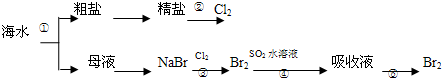

| A. | 上述工艺流程中涉及到化合、分解、复分解和置换反应 | |
| B. | ①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2 | |
| C. | ③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2 | |
| D. | ④中反应的离子方程式为SO2+Br2+2H2O═4H++SO42-+2Br- |
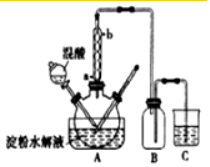
7.下列实验装置或操作能达到实验目的是( )


| A. | 制取Fe(OH)2的装置及操作 | |
| B. | 某溶液用盐酸酸化后再滴加硝酸钡溶液,检验溶液中是否含有SO42- | |
| C. | 向滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后溶液的红色褪去,可证明Na2CO3溶液显碱性是由于CO32-水解造成的 | |
| D. | 将氯化铁饱和滚液与稀氨水混合,加热至沸腾,制备Fe(OH)3胶体 |
14.碱式碳酸铜Cu2(OH)2CO3又称为铜绿,属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
4.对于平衡体系mA(g)+nB(g)?pC(g)+qD(g)△H=bkJ/mol.下列结论中错误的是( )
| A. | 若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q | |
| B. | 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | |
| C. | 若m+n=p+q,则向含有amol气体的平衡体系中再加入amol的B,达到新平衡时,气体的总物质的量等于2amol | |
| D. | 保持其它条件不变,如升高温度,D的体积分数增大,说明该反应的△H<0 |
11.已知R元素的某种同位素能形成化合物AmRn,其中A的化合价为+n.该化合物中一个R微粒的核外电子数为a,核内中子数为b,则该同位素的原子符号是( )
| A. | ${\;}_{a+m}^{b+m+n}R$ | B. | ${\;}_{a+m}^{b+a-m}R$ | C. | ${\;}_{a}^{b+a}R$ | D. | ${\;}_{a-m}^{a-m+b}R$ |
8.常温下,有甲、乙两份体积为1L,浓度均为0.1mol•L-1的醋酸溶液,其pH为3,①甲用蒸馏水稀释100倍后,溶液的pH变为x;②乙与等体积、浓度为0.2mol•L-1的NaOH混合,在混合液中:n(CH3COO-)+n(OH-)-n(H+)=y mol,x、y的正确答案组合为( )
| A. | 5; 0.1 | B. | 5; 0.2 | C. | 3<x<5; 0.1 | D. | 3<x<5; 0.2 |