籾朕坪否
18⤴和双蛎峰屎鳩旺拝嗤咀惚購狼議頁↙ ⇄| 僉𡸴 | 蛎峰↔ | 蛎峰Å |
| A | SO2嗤働易來 | SO2辛聞粤邦擁弼 |
| B | SiO2嗤擬窮來 | SiO2辛喘噐崙姥高擬亘略 |
| C | 狽剳晒汰辛嚥冦磨郡哘 | 狽剳晒汰辛喘噐嵶粗慮磨狛謹 |
| D | 絶議敵嵓磨嚥鑓音窟伏郡哘 | 辛參喘鑓菓概刈塰敵嵓磨 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
蛍裂 A⤴聞粤邦擁弼悶孖阻屈剳晒葬議珊圻來◉
B⤴SiO2唱悶斤高醤嗤畠郡符恬喘⇧嬬勧弓高佚催◉
C⤴慮磨嶄根嗤冦磨◉
D⤴絶議敵嵓磨嚥鑓氏窟伏緊晒⤴
盾基 盾⦿A⤴汽嵎粤嚥屈剳晒葬嬬窟伏剳晒珊圻郡哘⇧屈剳晒葬辛聞粤邦擁弼悶孖阻珊圻來⇧絞A危列◉
B⤴SiO2唱悶斤高醤嗤畠郡符恬喘⇧嬬勧弓高佚催⇧侭參SiO2辛喘噐崙姥高擬亘略⇧絞B危列◉
C⤴慮磨嶄根嗤冦磨⇧狽剳晒汰辛嚥冦磨郡哘⇧侭參狽剳晒汰辛喘噐嵶粗慮磨狛謹⇧絞C屎鳩◉
D⤴絶議敵嵓磨嚥鑓氏窟伏緊晒⇧壓鑓議燕中侘撹崑畜議剳晒弔⇧嬬隠擦坪何署奉音勣磨郡哘⇧侭參辛參喘鑓菓概刈塰敵嵓磨⇧絞D危列◉
絞僉C⤴
泣得 云籾忝栽深臥圷殆晒栽麗岑紛⇧葎互深械需籾侏⇧迦嶷噐僥伏議蛍裂嬬薦才圷殆晒栽麗岑紛議忝栽尖盾才塰喘議深臥⇧廣吭屢購児粥岑紛議持拙⇧佃業音寄⤴

膳楼過狼双基宛
屢購籾朕
8⤴25≧扮⇧和双嗤購卑匣嶄裏腺議麗嵎議楚敵業購狼屎鳩議頁↙ ⇄
| A⤴ | 0.1mol/L閑磨墜卑匣20ml嚥0.1mol/L冦磨10mL詞栽朔議卑匣嶄⦿c↙CH3COO-⇄﹅c↙Cl-⇄﹅c↙H+⇄﹅c↙CH3COOH⇄ | |
| B⤴ | 麗嵎議楚敵業屢吉議〙NH4Cl〖↙NH4⇄2SO4〗NH4Al↙SO4⇄2眉嶽卑匣嶄⇧c↙NH4+⇄喇寄欺弌議乏會葎⦿〗﹅〖﹅〙 | |
| C⤴ | 敵業葎O⤴lmol/L議〙葦邦、〖C6H5ONa卑匣、〗Na2CO3卑匣、∠NaHCO3卑匣⇧pH議寄弌乏會⦿〙﹅∠﹅〗﹅〖﹅ | |
| D⤴ | NaHCO3卑匣嶄⦿c↙H+⇄+c↙H2CO3⇄=c↙CO32-⇄+c↙OH-⇄ |
9⤴晒僥嚥芙氏、伏試畜俳屢購⤴斤和双孖嵆賜並糞議盾瞥屎鳩議頁↙ ⇄
| 僉𡸴 | 孖嵆賜並糞 | 盾瞥 |
| A | 喘犯議付珠卑匣牢肇嗟麟 | Na2CO3辛岷俊才嗟麟郡哘 |
| B | 働易頚壓腎賑嶄消崔延嵎 | 働易頚嶄議CaCl2嚥腎賑嶄議CO2郡 哘伏撹CaCO3 |
| C | 仏景扮⇧課直子↙嗤丼撹蛍葎K2CO3⇄音嬬 嚥NH4Cl詞栽聞喘 | K2CO3嚥NH4Cl郡哘伏撹葦賑氏週詰 景丼 |
| D | FeCl3卑匣辛喘噐有嵎咫泡㞍揃医崙恬 | FeCl3嬬貫根嗤Cu2+議卑匣嶄崔算竃有 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
6⤴譜NA葎唖懸紗蟻袋械方峙⇧和双嗤購偃峰屎鳩議頁↙ ⇄
| A⤴ | 械梁械儿和⇧30 g厰莱賑悶嶄侭根嗤議慌勺囚方朕葎6NA | |
| B⤴ | 炎彈彜趨和⇧0.4 g D2嶄侭根嶄徨議方朕葎0.2NA | |
| C⤴ | 械梁和⇧1 L pH=12議葦邦卑匣嶄根嗤NH4+方朕葎0.01NA | |
| D⤴ | 炎彈彜趨和⇧腹嗤11.2 L NO2議畜液否匂嶄紀圻徨方葎0.5NA |
13⤴和双光怏議曾嶽麗嵎壓卑匣嶄議郡哘⇧辛喘揖匯宣徨圭殻塀燕幣議頁↙ ⇄
| A⤴ | 狽剳晒有嚥冦磨◉狽剳晒有嚥閑磨 | |
| B⤴ | BaCl2卑匣嚥Na2SO4卑匣◉Ba↙OH⇄2卑匣嚥H2SO4卑匣 | |
| C⤴ | NaHCO3卑匣嚥冦磨◉Na2CO3嚥冦磨 | |
| D⤴ | 墳子墳嚥嵓磨郡哘◉墳子墳嚥冦磨 |
3⤴和双卑匣嶄柁宣徨敵業嚥50mL 1mol/L柁晒汰卑匣嶄柁宣徨敵業屢吉議頁↙ ⇄
| A⤴ | 150mL1mol/L議柁晒墜卑匣 | B⤴ | 75mL2mol/L議柁晒錻卑匣 | ||
| C⤴ | 150mL3mol/L議柁晒蛇卑匣 | D⤴ | 75mL1mol/L議柁晒冉鑓卑匣 |
7⤴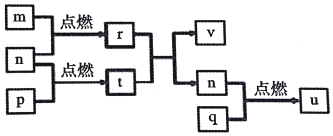 玉巓豚麼怛圷殆X、Y、Z、W議圻徨會方卆肝奐寄⤴膨嶽圷殆侘撹議汽嵎卆肝葎m、n、p、q⇧r、t、u頁宸乂圷殆怏撹議屈圷晒栽麗⇧凪嶄u葎侘撹磨嚏議麼勣麗嵎岻匯◉25≧扮⇧0.01mol•L-1議v卑匣嶄⦿$\frac{c↙O{H}^{-}⇄}{c↙{H}^{+}⇄}$=1.0〜1010⤴貧峰麗嵎議廬晒購狼泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
玉巓豚麼怛圷殆X、Y、Z、W議圻徨會方卆肝奐寄⤴膨嶽圷殆侘撹議汽嵎卆肝葎m、n、p、q⇧r、t、u頁宸乂圷殆怏撹議屈圷晒栽麗⇧凪嶄u葎侘撹磨嚏議麼勣麗嵎岻匯◉25≧扮⇧0.01mol•L-1議v卑匣嶄⦿$\frac{c↙O{H}^{-}⇄}{c↙{H}^{+}⇄}$=1.0〜1010⤴貧峰麗嵎議廬晒購狼泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
 玉巓豚麼怛圷殆X、Y、Z、W議圻徨會方卆肝奐寄⤴膨嶽圷殆侘撹議汽嵎卆肝葎m、n、p、q⇧r、t、u頁宸乂圷殆怏撹議屈圷晒栽麗⇧凪嶄u葎侘撹磨嚏議麼勣麗嵎岻匯◉25≧扮⇧0.01mol•L-1議v卑匣嶄⦿$\frac{c↙O{H}^{-}⇄}{c↙{H}^{+}⇄}$=1.0〜1010⤴貧峰麗嵎議廬晒購狼泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄
玉巓豚麼怛圷殆X、Y、Z、W議圻徨會方卆肝奐寄⤴膨嶽圷殆侘撹議汽嵎卆肝葎m、n、p、q⇧r、t、u頁宸乂圷殆怏撹議屈圷晒栽麗⇧凪嶄u葎侘撹磨嚏議麼勣麗嵎岻匯◉25≧扮⇧0.01mol•L-1議v卑匣嶄⦿$\frac{c↙O{H}^{-}⇄}{c↙{H}^{+}⇄}$=1.0〜1010⤴貧峰麗嵎議廬晒購狼泌夕侭幣⤴和双傍隈屎鳩議頁↙ ⇄| A⤴ | 圻徨磯抄議寄弌⦿W﹅Z﹅Y﹅X | |
| B⤴ | Z蛍艶嚥Y、W怏撹議晒栽麗嶄晒僥囚窃侏辛嬬屢揖 | |
| C⤴ | v嬬雙崙邦議窮宣遇u嬬陥序邦議窮宣 | |
| D⤴ | 娚嗤q議編砿辛喘焼娼牢脚 |
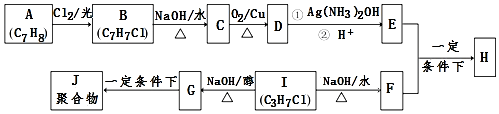
 ⤴
⤴ ⤴
⤴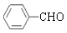 +2Ag↙NH3⇄2OH$\stackrel{@}{★}$
+2Ag↙NH3⇄2OH$\stackrel{@}{★}$ +2Ag◎+3NH3+H2O⤴
+2Ag◎+3NH3+H2O⤴