题目内容
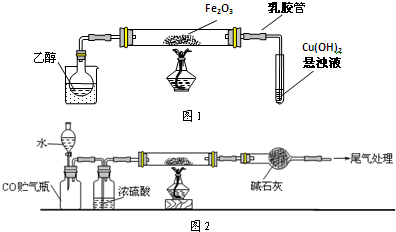
(1)实验证明,硫化铜与硫酸铁在细菌作用下,在潮湿多雨的夏季,成为硫酸和硫酸盐而溶解于水,这就是废石堆渗沥水,矿坑水成为重金属酸性废水的主要原因,试写出配平的化学方程式.
(2)从金矿中提取金,传统的也是效率极高的方法是氰化法.氰化法提金是在氧存在下氰化物盐类可以溶解金.试写出配平的化学方程式.
(3)对二乙苯在酸性高锰酸钾溶液中被氧化并有气体产生,试写出配平的反应式.
(2)从金矿中提取金,传统的也是效率极高的方法是氰化法.氰化法提金是在氧存在下氰化物盐类可以溶解金.试写出配平的化学方程式.
(3)对二乙苯在酸性高锰酸钾溶液中被氧化并有气体产生,试写出配平的反应式.
考点:铜金属及其重要化合物的主要性质,金属冶炼的一般原理,有机化学反应的综合应用
专题:元素及其化合物,有机反应
分析:(1)依据题意得出反应物为硫化铜和硫酸铁、水,条件是细菌,生成物是硫酸和硫酸盐,据此写出即可;
(2)反应物是氧气与氰化钠(或氰化钾)反应生成含金的化合物,据此写出即可;
(3)依据高锰酸钾将甲苯氧化为甲酸,据此写出即可.
(2)反应物是氧气与氰化钠(或氰化钾)反应生成含金的化合物,据此写出即可;
(3)依据高锰酸钾将甲苯氧化为甲酸,据此写出即可.
解答:
(1)解:反应物为硫化铜和硫酸铁、水,条件是细菌,生成物是硫酸和硫酸亚铁,化学反应方程式为:CuS+4Fe2(SO4)3+4H2O
CuSO4+8FeSO4+4H2SO4,
故答案为:CuS+4Fe2(SO4)3+4H2O
CuSO4+8FeSO4+4H2SO4;
(2)依据题意得出反应物为金、氰化钠、氧气和水,生成物为含金的盐,化学反应方程式为:4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH,
故答案为:4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH;
(3)依据高锰酸钾与甲苯生成苯甲酸,得出对二乙苯与高锰酸钾反应生成对二甲酸,有气体生成,气体为二氧化碳,化学反应方程式为:5CH3CH2- -CH2CH3+24KMnO4+36H2SO4=5HOOC-
-CH2CH3+24KMnO4+36H2SO4=5HOOC- -COOH+12K2SO4+24MnSO4+10CO2↑56H2O,
-COOH+12K2SO4+24MnSO4+10CO2↑56H2O,
故答案为:5CH3CH2- -CH2CH3+24KMnO4+36H2SO4=5HOOC-
-CH2CH3+24KMnO4+36H2SO4=5HOOC- -COOH+12K2SO4+24MnSO4+10CO2↑56H2O.
-COOH+12K2SO4+24MnSO4+10CO2↑56H2O.
| ||
故答案为:CuS+4Fe2(SO4)3+4H2O
| ||
(2)依据题意得出反应物为金、氰化钠、氧气和水,生成物为含金的盐,化学反应方程式为:4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH,
故答案为:4Au+8NaCN+2H2O+O2=4NaAu(CN)2+4NaOH;
(3)依据高锰酸钾与甲苯生成苯甲酸,得出对二乙苯与高锰酸钾反应生成对二甲酸,有气体生成,气体为二氧化碳,化学反应方程式为:5CH3CH2-
 -CH2CH3+24KMnO4+36H2SO4=5HOOC-
-CH2CH3+24KMnO4+36H2SO4=5HOOC- -COOH+12K2SO4+24MnSO4+10CO2↑56H2O,
-COOH+12K2SO4+24MnSO4+10CO2↑56H2O,故答案为:5CH3CH2-
 -CH2CH3+24KMnO4+36H2SO4=5HOOC-
-CH2CH3+24KMnO4+36H2SO4=5HOOC- -COOH+12K2SO4+24MnSO4+10CO2↑56H2O.
-COOH+12K2SO4+24MnSO4+10CO2↑56H2O.
点评:本题主要考查的是学生依据题给信息,写化学反应方程式的能力,题目难度较大,找准反应物、生成物是解决本题的关键.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的数值,则下列说法中不正确的是( )
①2.24L氖气含有NA个电子,
②18gD2O中所含的中子数为10NA,
③标准状况下,11.2LSO3 含有的分子数为0.5NA,
④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,
⑤在1L 0.1mol/L的碳酸钠溶液中,CO32-总数小于0.1NA.
①2.24L氖气含有NA个电子,
②18gD2O中所含的中子数为10NA,
③标准状况下,11.2LSO3 含有的分子数为0.5NA,
④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,
⑤在1L 0.1mol/L的碳酸钠溶液中,CO32-总数小于0.1NA.
| A、①②③⑤ | B、①④⑤ |
| C、①②③ | D、②③⑤ |
在标准状况下,下列物质的体积最大的是( )
| A、3g H2 |
| B、1mol SO2 |
| C、36g H2O |
| D、6.02×1022个N2 |
铜片放入热的稀硫酸中无明显现象,当加入下列哪种物质后现象有明显变化的是( )
| A、NaNO3 |
| B、HCl |
| C、NaOH |
| D、KCl |
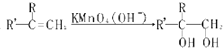


 RCHO
RCHO