题目内容
13.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )| A. | W、Y、Z的非金属性大小顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | W、Z形成的某化合物常可用作萃取剂 | |
| D. | WY2分子中既有非极性键又有极性键 |
分析 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则Z为Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,据此进行解答.
解答 解:短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则Z为Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,
A.同主族自上而下电负性减弱,Y若为Si元素,则非金属性C>Si,故A错误;
B.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Al>Y>Cl>C,即原子半径大小顺序可能是X>Y>Z>W,故B错误;
C.W为C,Z为Cl元素,二者形成四氯化碳,四氯化碳为常见的有机溶剂,可用作萃取剂,故C正确;
D、Y为Si或P或S元素,W为C元素,WY2分子为CS2,其分子中只含有极性键,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的综合应用,题目难度中等,能根据题意正确判断元素是解本题的关键,要注意把握对应单质和化合物的性质,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
3.下列有机物发生的反应属于还原反应的是( )
| A. | 乙醛与新制氢氧化铜反应 | B. | 油脂的氢化反应 | ||
| C. | 乙酸乙酯酸性条件下水解 | D. | 油脂的皂化反应 |
4.下列变化中,吸收的热量用于克服分子间作用力的是( )
| A. | 液溴受热变成溴蒸气 | B. | 加热金刚石使之熔化 | ||
| C. | 加热食盐使之熔化 | D. | 加热碘化氢使之分解 |
1.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( )


| A. | 单斜硫和正交硫互为同素异形体 | |
| B. | 单斜硫比正交硫稳定 | |
| C. | 两种硫的燃烧反应均为放热反应 | |
| D. | S(s,单斜)=S(s,正交)△H=-0.33 kJ•mol-1 |

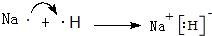 ;
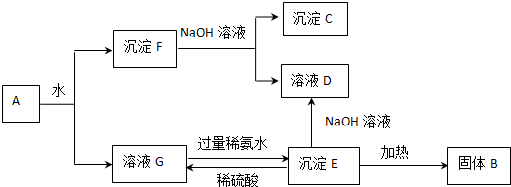
;
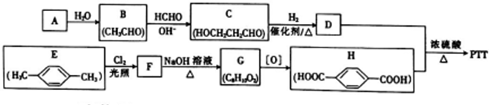
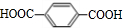 +n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$
+n HOCH2CH2CH2OH$→_{△}^{浓硫酸}$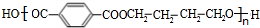 +(2n-1)H2O,该反应的反应类型为缩聚反应.
+(2n-1)H2O,该反应的反应类型为缩聚反应.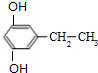 (填结构简式,任写一种)
(填结构简式,任写一种)