题目内容
17.以极性键结合的多原子分子,分子是否有极性取决于分子的空间构型.下列分子都属于含极性键的非极性分子的是( )| A. | CO2 H2O | B. | NH3 BCl3 | C. | PCl3 CH4 | D. | PCl5 CH4 |
分析 极性分子中正负电荷的中心不重合,具有一定的极性,极性分子是由极性键构成的结构不对称的分子,据此判断.
解答 解:A.二氧化碳结构为O=C=O,结构对称,正负电荷的中心重合,属于非极性分子,H2O为V形分子,结构不对称,正负电荷的中心不重合,属于极性分子,故A不选;
B.NH3为三角锥形,结构不对称,正负电荷的中心不重合,属于极性分子,BCl3分子,为正三角形,结构对称,正负电荷的中心重合,属于非极性分子,故B不选;
C.PCl3为三角锥形,结构不对称,正负电荷的中心不重合,属于极性分子,CH4为正四面体结构,结构对称,正负电荷的中心重合,属于非极性分子,故C不选;
D.PCl5为三角双锥结构,结构对称,正负电荷的中心重合,属于非极性分子,CH4为正四面体结构,结构对称,正负电荷的中心重合,属于非极性分子,故D选.
故选D.
点评 本题考查极性分子和非极性分子,熟悉常见元素之间的成键是解答本题的关键,注意化学键与分子的极性的关系来分析解答即可,难度不大.

练习册系列答案
相关题目
8.下列各组物质中,属于同素异形体的是( )
| A. | S2、S4 | B. | 碘晶体、碘蒸气 | ||
| C. | H、D | D. | ${\;}_{8}^{16}$O2、${\;}_{8}^{18}$O2 |
12.配制50g溶质的质量分数为 6%的氯化钠溶液,不需要的仪器是( )
| A. | 蒸发皿 | B. | 玻璃棒 | C. | 烧杯 | D. | 量筒 |
9.稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域.一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如图1:
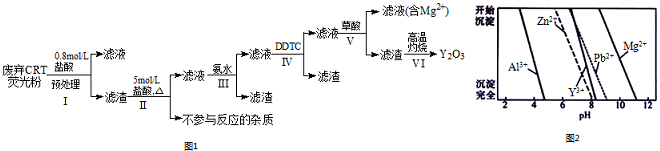
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;
②不同离子沉淀的pH如图2所示.
(1)步骤I中进行原料预处理的目的为除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量等.(答两点)
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]=8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.

已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;
| 阶段/含量%/成分 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
(1)步骤I中进行原料预处理的目的为除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量等.(答两点)
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]=8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.
6.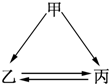 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
①Fe
②HNO3
③Na
④Si.
 \如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
\如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①Fe
②HNO3
③Na
④Si.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
7.下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是( )
| A. | SO2、H2S、Cl2 | B. | SO2、O2、NH3 | C. | NO、O2、H2 | D. | SO2、CO2、O2 |
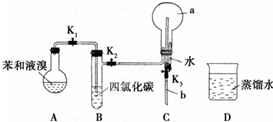
 ,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.
,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.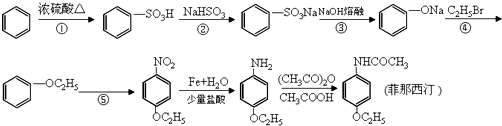
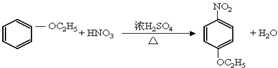 ;
;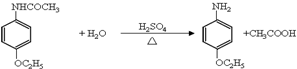 ;
;