题目内容
15.下列关于反应热的叙述正确的是( )| A. | 反应热就是反应发出的热量 | |
| B. | 由C(s)+$\frac{1}{2}$O2(g)═CO(g)的反应热为110.5kJ•mol-1,可知碳的燃烧热为110.5 kJ•mol-1 | |
| C. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 | |
| D. | 1mol NaOH分别和1mol CH3COOH、1mol HNO3反应放出的热量:CH3COOH<HNO3 |
分析 A、反应热是指反应过程中所放出或吸收的热;
B.燃烧热是指1mol可燃物完全燃烧生成稳定氧化物放出的热量;
C.化学反应的焓变决定于反应物与生成物的能量差;
D.强酸强碱稀溶液完全反应生成1mol水放热的热量为中和热,醋酸是弱酸存在电离平衡,电离过程是吸热过程;
解答 解:A、反应过程中吸收的热都也是反应热,故A错误;
B.碳的燃烧热是弱酸生成二氧化碳放出的热量,一氧化碳是不稳定的氧化物,故B错误;
C.化学反应的焓变决定于反应物与生成物的能量差,反应热的大小与反应物所具有的能量和生成物所具有的能量有关,故C错误;
D.醋酸是弱酸存在电离平衡,电离过程是吸热过程,1mol NaOH分别和1mol CH3COOH、1mol HNO3反应放出的热量:CH3COOH<HNO3,故D正确;
故选D.
点评 本题考查了化学反应能量变化,燃烧热、中和热概念的理解应用,注意反应焓变的计算方法,题目较简单.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
6.钛号称“崛起的第三金属”,因具有密度小、强度大、无磁性等优良的机械性能,被广泛应用于军事、医学等领域.已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是( )
| A. | 上述钛原子中,中子数不可能为22 | |
| B. | 钛元素在周期表中处于第四周期ⅡB族 | |
| C. | 钛原子的外围电子层排布为3d24s2 | |
| D. | 钛元素位于元素周期表的d区,是过渡元素 |
3.已知25℃时,有关弱酸的电离平衡常数如下表:
则等物质的量浓度的a.CH3COONa,b.NaCN,c.Na2CO3,d.NaHCO3溶液的pH由大到小的顺序是
c>b>d>a(填编号),0.18mol•L-1 CH3COONa的pH约为9.
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数Ka | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
c>b>d>a(填编号),0.18mol•L-1 CH3COONa的pH约为9.
10.下列与金属腐蚀有关的说法,正确的是( )
| A. | 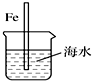 图中,插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. |  图中,发生吸氧腐蚀 | |
| C. | 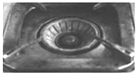 图中,燃烧灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 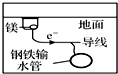 图中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁相当于原电池的正极 |
4.自然环境与人们的生活息息相关.下列有关环境的说法不正确的是( )
| A. | 氟利昂(CCl2F2)因破坏大气臭氧层,会导致“温室效应” | |
| B. | 生活污水中所含的氮、磷化合物是植物营养素,但会导致水体污染 | |
| C. | 废旧电池的回收,其主要目的是为了保护环境 | |
| D. | 淀粉餐具被认为是最有发展前景的一次性餐具,可有利于保护环境 |
5.下列物质中,只能与NaOH溶液作用,不能与盐酸作用的是( )
| A. | KHSO4 | B. | (NH4)2CO3 | C. | NaHCO3 | D. | NH4HCO3 |