题目内容
18.某无色溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是( )| A. | Fe2+、Cl-、Na+、NO3- | B. | Na+、Ba2+、Cl-、NO3- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | Na+、K+、AlO2-、SO42- |
分析 溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,能溶解Al(OH)3的溶液中存在大量氢离子或氢氧根离子,
A.亚铁离子为有色离子,亚铁离子与氢氧根离子反应,硝酸根离子在酸性条件下能够氧化亚铁离子;
B.四种离子之间不反应,都是无色离子,都不与氢离子和氢氧根离子反应;
C.碳酸氢根离子与氢离子和氢氧根离子反应;
D.偏铝酸根离子与氢离子反应.
解答 解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,能溶解Al(OH)3的溶液中存在大量氢离子或氢氧根离子,
A.Fe2+为有色离子,Fe2+与氢氧根离子反应,酸性溶液中Fe2+、NO3-发生氧化还原反应,在溶液中一定不能大量共存,故A错误;
B.Na+、Ba2+、Cl-、NO3-之间不发生反应,都是无色离子,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.HCO3-与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.AlO2-与氢离子反应,在酸性溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
9.在下列变化过程中,被破坏的微粒间作用力正确的是( )
| A. | 冰融化一一共价键 | B. | 二氧化硅熔融--范德华力 | ||
| C. | 氢氧化钠溶于水--离子键、共价键 | D. | 硫酸氢钠溶于水--离子键、共价键 |
3.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
| A. | Na2CO3 NaCl NaOH | B. | NaOH NaCl Na2CO3 | ||
| C. | NaCl NaOH Na2CO3 | D. | NaCl Na2CO3 NaOH |
10.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),能说明该可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 体系的压强不再发生变化 | |
| B. | v(CO2)=v(H2O) | |
| C. | 生成n mol CH3OH的同时生成n mol H2O | |
| D. | 3 mol H-H键断裂的同时断裂2 mol H-O键 |
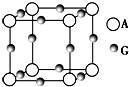 已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(KJ•mol-1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外价电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、F的原子均有三个能层,C原子的第一至第四电离能(KJ•mol-1)分别为578、1 817、2 745、11 575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q.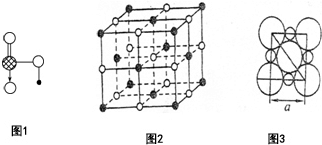 (1)Na、Cu、Si、H、C、N六种元素,其对应单质的熔点按照A、B、C、D、E、F的顺序依次升高,其中C、D均是热和电的良导体.
(1)Na、Cu、Si、H、C、N六种元素,其对应单质的熔点按照A、B、C、D、E、F的顺序依次升高,其中C、D均是热和电的良导体.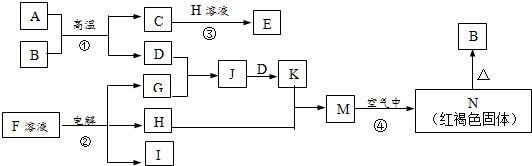
 .
.