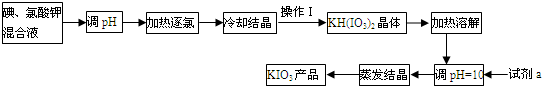
题目内容
 利用如图装置可验证同主族元素非金属性的变化规律
利用如图装置可验证同主族元素非金属性的变化规律(1)仪器B的名称为
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加
(4)为了达到下表中的实验要求,请从供选择的化学试剂及实验方法中选出合适的字母标号填入对应的空格中.
| 题号 | 实 验 要 求 | 答案 |
| ① | 从碘水中提取碘单质 | |
| ② | 提纯混有少混NaCl的KNO3 | |
| ③ | 鉴别NaCl和KCl | |
| ④ | 检验自来水中残余氯分子 |
A.加热灼烧,观察
B.在较高温度下溶于水配成浓溶液,再冷却结晶
C.加入四氯化碳萃取
D.将样品滴在淀粉碘化钾试纸上.
考点:性质实验方案的设计,非金属在元素周期表中的位置及其性质递变的规律
专题:实验设计题
分析:(1)仪器B的名称为锥形瓶;尾气处理装置中,有缓冲装置的能防止倒吸;
(2)浓盐酸和酸性高锰酸钾溶液发生氧化还原反应生成Cl2,Cl2具有氧化性,能氧化I-生成I2,碘遇淀粉试液变蓝色;Cl2和碱反应生成盐,可以用碱液吸收氯气;
(3)非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;为防止HCl干扰,应该加入一个装置吸收HCl且不能溶解CO2;
(4)碘在水中的溶解度小于在有机溶剂中的溶解度,可以采用萃取方法提取碘水中的碘;
NaCl、KNO3随着温度变化其溶解度变化不同,可以采用结晶方法分离;
NaCl、KCl可以采用焰色反应鉴别;
氯气有强氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色.
(2)浓盐酸和酸性高锰酸钾溶液发生氧化还原反应生成Cl2,Cl2具有氧化性,能氧化I-生成I2,碘遇淀粉试液变蓝色;Cl2和碱反应生成盐,可以用碱液吸收氯气;
(3)非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;为防止HCl干扰,应该加入一个装置吸收HCl且不能溶解CO2;
(4)碘在水中的溶解度小于在有机溶剂中的溶解度,可以采用萃取方法提取碘水中的碘;
NaCl、KNO3随着温度变化其溶解度变化不同,可以采用结晶方法分离;
NaCl、KCl可以采用焰色反应鉴别;
氯气有强氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色.
解答:
解:(1)仪器B的名称为锥形瓶;尾气处理装置中,有缓冲装置的能防止倒吸,干燥管有缓冲作用,所以能防止倒吸,故答案为:锥形瓶;倒吸;
(2)浓盐酸和酸性高锰酸钾溶液发生氧化还原反应生成Cl2,Cl2具有氧化性,能氧化I-生成I2,碘遇淀粉试液变蓝色,C装置中看到的现象是溶液变蓝色;Cl2和碱反应生成盐,可以用碱液吸收氯气,如NaOH溶液,
故答案为:变蓝;NaOH;
(3)非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,要证明C元素非金属性大于Si元素,只要证明碳酸酸性大于硅酸即可,所以C中加入Na2SiO3;为防止HCl干扰,应该加入一个装置吸收HCl且不能溶解CO2,如饱和NaHCO3溶液,故答案为:Na2SiO3;饱和NaHCO3;
(4)碘在水中的溶解度小于在有机溶剂中的溶解度,可以采用萃取方法提取碘水中的碘,如用CCl4作萃取剂萃取碘水中的碘,故选C;
NaCl、KNO3随着温度变化其溶解度变化不同,可以采用冷却结晶方法分离,故选B;
NaCl、KCl都易溶于水,只要金属元素不同,可以采用焰色反应鉴别,故选A;
氯气有强氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色,所以可以用湿润的淀粉碘化钾试纸检验残余氯分子,故选D.
(2)浓盐酸和酸性高锰酸钾溶液发生氧化还原反应生成Cl2,Cl2具有氧化性,能氧化I-生成I2,碘遇淀粉试液变蓝色,C装置中看到的现象是溶液变蓝色;Cl2和碱反应生成盐,可以用碱液吸收氯气,如NaOH溶液,
故答案为:变蓝;NaOH;
(3)非金属的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,要证明C元素非金属性大于Si元素,只要证明碳酸酸性大于硅酸即可,所以C中加入Na2SiO3;为防止HCl干扰,应该加入一个装置吸收HCl且不能溶解CO2,如饱和NaHCO3溶液,故答案为:Na2SiO3;饱和NaHCO3;
(4)碘在水中的溶解度小于在有机溶剂中的溶解度,可以采用萃取方法提取碘水中的碘,如用CCl4作萃取剂萃取碘水中的碘,故选C;
NaCl、KNO3随着温度变化其溶解度变化不同,可以采用冷却结晶方法分离,故选B;
NaCl、KCl都易溶于水,只要金属元素不同,可以采用焰色反应鉴别,故选A;
氯气有强氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色,所以可以用湿润的淀粉碘化钾试纸检验残余氯分子,故选D.
点评:本题考查性质实验方案设计、混合物的分离和提纯等知识点,明确实验原理是解本题关键,知道常见仪器的作用、常见物质的性质,知道常见物质分离和提纯方法,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、将钠投入硫酸铜溶液中只有紫红色固体析出 |
| B、过氧化钠投入硫酸亚铁溶液中出现白色沉淀 |
| C、氨水滴入氯化铝溶液中先出现白色沉淀后溶解 |
| D、饱和氯化钙溶液加入浓氢氧化钠溶液出现白色沉淀 |
下列说法不正确的是( )
A、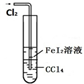 可以用于比较Fe3+、I2、Cl2的氧化性强弱 |
B、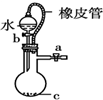 橡皮管的作用是使水能顺利流下 |
C、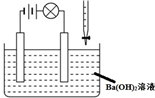 若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 |
D、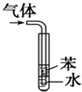 用于吸收HCl气体能防倒吸 |
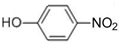 ⑥
⑥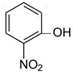 ⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl
⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl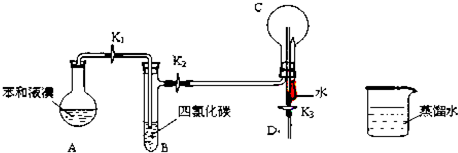
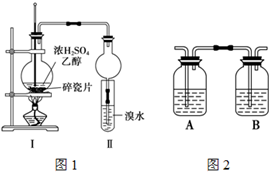 某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.
某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.