题目内容
11.某混合溶液含有的溶质为硫酸钠、氯化钠、硫酸镁,已知c(SO42-)=0.2mol/L,c(Na+)=0.1mol/L,c(Cl-)=0.2mol/L,则镁离子的浓度为0.25mol/L.分析 混合溶液呈电中性,根据电荷守恒:c(Cl-)+2(SO42-)=c(Na+)+2c(Mg2+),据此计算.
解答 解:混合溶液呈电中性,根据电荷守恒有:c(Cl-)+2(SO42-)=c(Na+)+2c(Mg2+),故:
0.2mol/L+2×0.2mol/L=0.1mol/L+2c(Mg2+),解得:2c(Mg2+)=0.25mol/L,
故答案为:0.25mol/L.
点评 本题考查物质的量浓度的有关计算,难度中等,注意电解质混合溶液经常利用电荷守恒计算离子浓度.

练习册系列答案
相关题目
2.下列分子中,所有原子最外层均为 8 电子结构的是( )
| A. | CO2 | B. | BF3 | C. | LiCl | D. | NH3 |
6.表是周期表中的一部分,根据A-I的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne.
(2)A-I元素中,非金属性最强的元素与金属性最强的元素形成的物质是Na,该物质的熔点比干冰的熔点高(填“低”或“高”).
(3)比较D、E最高价氧化物的水化物酸性强弱HNO3>H2CO3.
(4)G、H的氢化物沸点较高的是HF,理由是HF分子间含氢键.
(5)A、E、H组成的常见物质的电子式为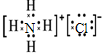 .
.
(6)用电子式表示E的氢化物的形成过程3H•+ →
→ .
.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | F | G | I | |||
| 3 | B | C | H |
(2)A-I元素中,非金属性最强的元素与金属性最强的元素形成的物质是Na,该物质的熔点比干冰的熔点高(填“低”或“高”).
(3)比较D、E最高价氧化物的水化物酸性强弱HNO3>H2CO3.
(4)G、H的氢化物沸点较高的是HF,理由是HF分子间含氢键.
(5)A、E、H组成的常见物质的电子式为
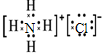 .
.(6)用电子式表示E的氢化物的形成过程3H•+
 →
→ .
.
3.火法炼汞是在不太高的温度下(450~800℃),将汞矿石或精矿进行焙烧,直接将汞还原呈气态分离出来,而后冷凝成液态汞.目前工业上制粗汞的流程如图:
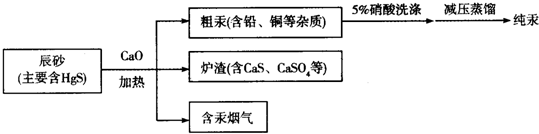
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 流程中加入氧化钙的目的是减少SO2的排放 | |
| B. | “辰砂”加热时发生反应:HgS+O2$\frac{\underline{\;\;△\;\;}}{\;}$Hg+SO2,该方法属于热分解法 | |
| C. | 洗涤粗汞时可用5%的盐酸代替5%的硝酸 | |
| D. | 含汞烟气中汞的含量很低,可以直接排放 |
7.下列化合物不能由对应元素单质直接化合生成的是( )
| A. | Cu2S | B. | FeCl3 | C. | Fe2S3 | D. | HCl |

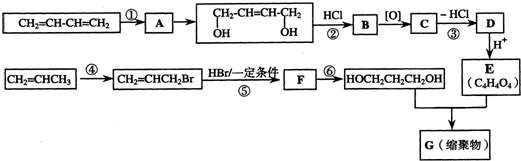
 .写出反应⑥的化学方程式:CH2BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2CH2OH+2NaBr.
.写出反应⑥的化学方程式:CH2BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2CH2OH+2NaBr.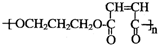 .
.
 H2O2:
H2O2: MgO:
MgO: N2:
N2: