题目内容
反应A+3B?2C在10℃时,v(B)=0.3mol?(L?s)-1,50℃时v(A)=25.6mol?(L?s)-1,若温度每升高10℃,反应速率增至原来的n倍,则n值为( )
| A、2 | B、3 | C、4 | D、5 |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:把10℃时的v(B)根据化学反应速率之比等于化学计量数之比换算成时v(A),此时10℃时的v(A)乘以n4等于50℃时v(A)=25.6mol?(L?s)-1.
解答:
解:把10℃时,v(A)=
×v(B)=
×0.3mol?(L?s)-1=0.1mol?(L?s)-1,0.1mol?(L?s)-1×n4=25.6mol?(L?s)-1,n=4,
故选:C.
| 1 |
| 3 |
| 1 |
| 3 |
故选:C.
点评:本题考查温度对反应速率的影响,把握信息中“温度每升高10℃,反应速率增大到原来的n倍”是解答本题的关键,注意速率之比等于化学计量数之比的应用,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列说法正确的是( )
| A、阴阳离子之间的相互吸引力称为离子键 |
| B、使阴阳离子结合形成化合物的吸引力,叫做离子键 |
| C、使阴阳离子结合形成化合物的静电作用,叫做离子键 |
| D、含有离子键的化合物一定是离子化合物 |
在反应3Cl2+6NaOH
5NaCl+NaClO3+3H2O中,氧化产物是( )
| ||
| A、Cl2 |
| B、NaCl |
| C、NaClO3 |
| D、H2O |
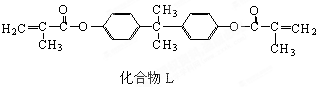 化合物L是一种能使人及动物的内分泌系统发生紊乱导致生育及繁殖异常的环境激素,它在一定条件下水解可生成双酚A和有机酸M.下列关于L、双酚A和M的叙述中正确的是( )
化合物L是一种能使人及动物的内分泌系统发生紊乱导致生育及繁殖异常的环境激素,它在一定条件下水解可生成双酚A和有机酸M.下列关于L、双酚A和M的叙述中正确的是( )| A、1mol L水解可以消耗2molNaOH |
| B、双酚A与苯酚互为同系物 |
| C、与M含相同官能团的同分异构体还有2种 |
| D、L、双酚A和M 均能与溴水发生加成反应 |
下列各组离子,在强碱性溶液中可以大量共存的是( )
①I-、AlO2-、Cl-、S2- ②Na+、K+、NH4+、Ba2+
③Br-、S2-、Cl-、CO32- ④SO32-、NO3-、SO42-、HCO3-.
①I-、AlO2-、Cl-、S2- ②Na+、K+、NH4+、Ba2+
③Br-、S2-、Cl-、CO32- ④SO32-、NO3-、SO42-、HCO3-.
| A、①③ | B、②④ | C、②③ | D、①④ |
下列各组气体通常情况下能大量共存,并且既能用浓硫酸干燥,又能用无水氯化钙干燥的是( )
| A、SO2、O2、HI |
| B、NH3、O2、N2 |
| C、NH3、CO2、HCl |
| D、H2、Cl2、O2 |
有“智力元素”之称的是( )
| A、Ca | B、O | C、I | D、F |
下列叙述正确的是( )
| A、Na2O与Na2O2都能和水反应生成碱,它们是碱性氧化物 |
| B、Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀 |
| C、Na2O2应保存于密封、干燥带玻璃塞的广口瓶中 |
| D、Na2O2可作供氧剂,而Na2O不行 |