题目内容
17.现有如下两个反应:A.NaOH+HCl═NaCl+H2O
B.Fe+H2SO4═FeSO4+H2↑
(1)上述能设计成原电池的反应是B(填序号,下同),写出其负极的电极反应式:Fe-2e-=Fe2+.
(2)上述不能设计成原电池的反应是A,其原因是应为非氧化还原反应,没有电子转移.
分析 自发进行的放热的氧化还原反应能设计成原电池;在氧化还原反应中失电子化合价升高的金属作负极、不如负极活泼的金属或导电的非金属作正极,得电子发生还原反应的电解质为该原电池电解质.
解答 解:(1)A中反应前后各元素化合价不变,所以不属于氧化还原反应,属于复分解反应,B中Fe元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以Fe发生氧化反应作负极,电极反应式为Fe-2e-=Zn2+,能设计成原电池,故答案为:B;Fe-2e-=Fe2+;
(2)能设计成的反应必须是自发进行的放热的氧化还原反应,A的反应为非氧化还原反应,没有电子转移,所以不能设计成原电池,故答案为:A;该反应为非氧化还原反应,没有电子转移.
点评 本题考查了原电池设计,明确原电池反应特点、正负极及电解质溶液的判断方法即可解答,在原电池反应中,一般来说,失电子化合价升高的金属单质作负极、得电子化合价降低的电解质为电解质溶液中的电解质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列过程不属于化学变化的是( )
| A. | 裂解 | B. | 裂化 | C. | 分馏 | D. | 干馏 |
5.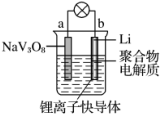 水系锂电池具有安全、环保和价格低廉等优点,成为当前电池研究领域的热点. 以钒酸钠(NaV3O8)为正极材料的电极反应式为NaV3O8+xLi++xe-═NaLixV3O8,则下列说法不正确的是( )
水系锂电池具有安全、环保和价格低廉等优点,成为当前电池研究领域的热点. 以钒酸钠(NaV3O8)为正极材料的电极反应式为NaV3O8+xLi++xe-═NaLixV3O8,则下列说法不正确的是( )
 水系锂电池具有安全、环保和价格低廉等优点,成为当前电池研究领域的热点. 以钒酸钠(NaV3O8)为正极材料的电极反应式为NaV3O8+xLi++xe-═NaLixV3O8,则下列说法不正确的是( )
水系锂电池具有安全、环保和价格低廉等优点,成为当前电池研究领域的热点. 以钒酸钠(NaV3O8)为正极材料的电极反应式为NaV3O8+xLi++xe-═NaLixV3O8,则下列说法不正确的是( )| A. | 放电时,负极的电极反应式:Li-e-═Li+ | |
| B. | 该电池可以用硫酸钠溶液作电解质 | |
| C. | 充电过程中阳极的电极反应式:NaLixV3O8-xe-═NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化 | |
| D. | 充电过程中Li+从阳极向阴极迁移 |
2.已知:以铜作催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛.某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液.左表给出甲醇、甲醛的沸点和水溶性:
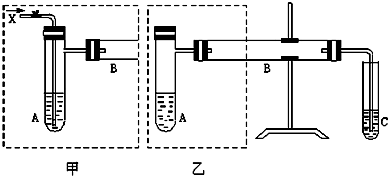
如图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示,请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是检查装置气密性.
(2)若按甲装置进行实验,则通入A的X是空气或氧气,B中发生反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(3)若按乙装置进行实验,则B管中应装入的物质是氧化铜,B中发生反应的化学方程式为CH3OH+CuO$→_{△}^{Cu}$Cu+HCHO+H2O.
(4)试管C中应装入的试剂是水.
(5)两套装置中都需要加热的仪器有A、B(填A、B、C).
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?甲(填“甲”或“乙”).
(7)请设计简单的实验,检验实验后C中所得液体确为甲醛溶液.简述所用试剂、操作、现象及结论.在试管中加入少量新制Cu(OH)2悬浊液,取少量C中液体滴入试管中,加热,有红色沉淀生成,证明C中所得液体为甲醛溶液.
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 与水混溶 |
| 甲醛 | -21 | 与水混溶 |

如图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示,请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是检查装置气密性.
(2)若按甲装置进行实验,则通入A的X是空气或氧气,B中发生反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(3)若按乙装置进行实验,则B管中应装入的物质是氧化铜,B中发生反应的化学方程式为CH3OH+CuO$→_{△}^{Cu}$Cu+HCHO+H2O.
(4)试管C中应装入的试剂是水.
(5)两套装置中都需要加热的仪器有A、B(填A、B、C).
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?甲(填“甲”或“乙”).
(7)请设计简单的实验,检验实验后C中所得液体确为甲醛溶液.简述所用试剂、操作、现象及结论.在试管中加入少量新制Cu(OH)2悬浊液,取少量C中液体滴入试管中,加热,有红色沉淀生成,证明C中所得液体为甲醛溶液.
9.下列电离方程式正确的是( )
| A. | H2CO3?2H++CO32- | B. | CH3COOH═CH3COO-+H+ | ||
| C. | AgCl═Ag++Cl- | D. | NaHCO3═Na++H++CO32- |
6.下列说法正确的是( )
| A. | 蔗糖、淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖 | |
| B. | 淀粉、纤维素、油脂、蛋白质都属于高分子化合物 | |
| C. | 利用油脂在酸性条件下的水解,可以制得甘油和肥皂 | |
| D. | 蛋白质水解的最终产物是氨基酸 |
7.三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3.则下列说法正确的是( )
| A. | NF3是氧化剂,H2O是还原剂 | |
| B. | NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 | |
| C. | 一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少空气污染 | |
| D. | 若生成0.2 mol HNO3,则转移0.2 mol电子 |