题目内容
7.下列离子方程式书写正确的是( )| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 稀硫酸与氢氧化钡溶液反应:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| C. | 用氨水溶液氯化银沉淀:Ag++2NH3•H2O═[Ag(NH3)2]++2H20 | |
| D. | Fe(OH)3 溶于过量的HI溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
分析 A.原子个数不守恒;
B.漏掉氢离子与氢氧根离子的反应;
C.氯化银为沉淀,保留化学式;
D.三价铁离子具有强的氧化性,能够氧化碘离子生成单质碘.
解答 解:A.钠与水反应离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故 A错误;
B.硫酸溶液与氢氧化钡溶液反应的离子方程式为Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓,故B错误;
C.用氨水溶解氯化银沉淀,氯化银不能拆开,正确的离子方程式为:AgCl+2NH3•H2O=[Ag(NH3)2]++2H2O+Cl-,故C错误;
D.Fe(OH)3 溶于过量的HI溶液,离子方程式:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O,故D正确.
故选:D.
点评 本题考查了离子方程式的书写判断,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,注意离子反应遵循客观事实、原子个数守恒、电荷守恒规律,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
7.a mol FeS与b mol FeO投入到V L、c mol•L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液的成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
(1)(a+b)×63g
(2)(a+b)×189g
(3)Vc-$\frac{(a+b)}{3}$mol
(4)Vc-$\frac{(9a+b)}{3}$mol.
(1)(a+b)×63g
(2)(a+b)×189g
(3)Vc-$\frac{(a+b)}{3}$mol
(4)Vc-$\frac{(9a+b)}{3}$mol.
| A. | (1)(3) | B. | (1)(4) | C. | (2)(3) | D. | (2)(4) |
2.化学与生活密切相关,下列说法正确的是( )
| A. | 晶体硅可用于制造光导纤维 | B. | 氯氧化钠用来治疗胃酸过多 | ||
| C. | 铝制容器可以用来贮运稀硝酸 | D. | 乙烯用作水果的催熟剂 |
19.下列实验事实和对实验事实的理论解释都正确的是( )
| 选项 | 实验事实 | 理论解释 |
| A | H2S的沸点比H2O的高 | H2S的范德华力大于H2O的范德华力 |
| B | 白磷为正四面体分子 | 白磷分子中P-P-P的键角是109.5° |
| C | 1体积水可以溶解700体积氨气 | 氨是极性分子且有氢键的影响 |
| D | 键的极性:H-O>N-H | 非金属性差异越大,键的极性越小 |
| A. | A | B. | B | C. | C | D. | D |
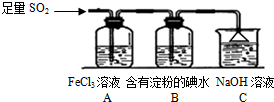 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: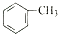 ;b.CH≡CCH3; c、
;b.CH≡CCH3; c、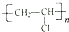
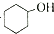 和
和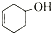 ,可选用b(填字母)
,可选用b(填字母)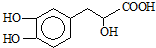
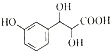 )与足量溴水反应所得产物的结构简式为
)与足量溴水反应所得产物的结构简式为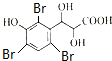 .
.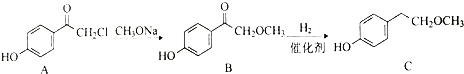
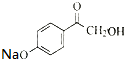 .
.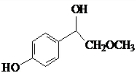 .
.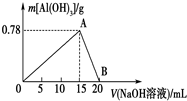 向20mL某物质的量浓度的AlCl3溶液中滴入2mol•L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向20mL某物质的量浓度的AlCl3溶液中滴入2mol•L-1NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加的NaOH溶液的体积(mL)关系如图所示,试回答下列问题: