题目内容
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、1 mol 氯气与足量氢氧化钠溶液完全反应,转移电子数目为2NA |
| B、14g氮气中含有14 NA个原子 |
| C、1L1.00 mol/L的Na2SO4溶液中Na+离子数目为2NA |
| D、11.2 L氢气中含有NA个氢原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氯气和氢氧化钠反应自身氧化还原反应,氯元素化合价从0价变化为-1价和+1价;
B、依据n=
计算物质的量,结合分子式计算原子数;
C、依据n=cV计算物质的量结合化学式计算离子数;
D、依据气体摩尔体积应用条件分析判断.
B、依据n=
| m |
| M |
C、依据n=cV计算物质的量结合化学式计算离子数;
D、依据气体摩尔体积应用条件分析判断.
解答:
解:A、1 mol 氯气与足量氢氧化钠溶液完全反应,转移电子数目为NA,故A错误;
B、14g氮气物质的量为0.5mol,分子中含有 NA个原子,故B错误;
C、1L1.00 mol/L的Na2SO4溶液中Na+离子数目=1L×1.00mol/L×NA×2=2NA,故C正确;
D、温度压强不知不能计算物质的量,故D错误;
故选C.
B、14g氮气物质的量为0.5mol,分子中含有 NA个原子,故B错误;
C、1L1.00 mol/L的Na2SO4溶液中Na+离子数目=1L×1.00mol/L×NA×2=2NA,故C正确;
D、温度压强不知不能计算物质的量,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要是氧化还原反应电子转移计算,气体摩尔体积的条件应用,题目难度中等.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
下列用来表示物质变化的化学用语中,正确的是( )
| A、钢铁腐蚀时负极发生的反应:Fe→Fe 3++3e- | ||
| B、明矾水解的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+ | ||
C、小苏打在水中的电离方程式:NaHCO3=Na++H++C
| ||
| D、1 g氢气在空气中完全燃烧生成液态水时放出285.8 kJ热量,其热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol |
已知:①C(s)+
O2(g)═CO(g)△H=-110.5kJ/mol??
②CO(g)+
O2(g)═CO2(g)△H=-283.0kJ/mol??
③H2(g)+
O2(g)═H2O(g)△H=-241.8kJ/mol??
下列说法正确的是( )
| 1 |
| 2 |
②CO(g)+
| 1 |
| 2 |
③H2(g)+
| 1 |
| 2 |
下列说法正确的是( )
| A、将2.4 g碳完全转化为水煤气,然后再燃烧,整个过程△H=-78.7 kJ/mol?? |
| B、H的燃烧热为241.8 kJ/mol?? |
| C、由反应②可推知,CO具有还原性而没有氧化性 |
| D、由反应③可知,反应过程中转移5 mol电子且生成液态水时放出的热量小于604.5 kJ |
根据下列实验事实,判断微粒氧化性大小顺序正确的是( )
①FeCl3溶液中滴入KI溶液,加CCl4振荡,CCl4层呈紫色
②FeCl2溶液中滴加氯水,再加KSCN溶液,呈红色
③KMnO4溶液中滴加盐酸.KMnO4溶液的紫色褪去.
①FeCl3溶液中滴入KI溶液,加CCl4振荡,CCl4层呈紫色
②FeCl2溶液中滴加氯水,再加KSCN溶液,呈红色
③KMnO4溶液中滴加盐酸.KMnO4溶液的紫色褪去.
| A、MnO-4>Fe3+>Cl2>I2 |
| B、Cl2>I2>Fe3+>MnO4 |
| C、MnO-4>Cl2>Fe3+>I2 |
| D、Fe3+>MnO-4>Cl2>I2 |
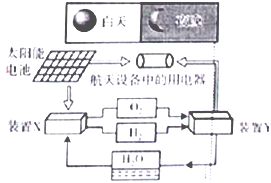 如图是一种航天器能量储存系统原理示意图.下列说法正确的是
如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )
| A、该系统中只存在3种形式的能量转化 |
| B、装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- |
| C、装置X能实现燃料电池的燃料和氧化剂再生 |
| D、该系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
由环己烷、乙醇、乙醚组成的混合物,经测定碳的质量分数为72%,则氧的质量分数为( )
| A、19.6% | B、17.8% |
| C、16% | D、14.2% |
 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A、5.4g水中含氢原子数为0.3NA |
| B、25℃,1L pH=12的氨水中,含有OH-的数目为0.1 NA |
| C、标准状况下,32g硫(结构如图)含S-S的数目为NA |
| D、在反应KIO3+6HI=3I2+KI+3H2O中,每生成l mol I2转移电子数为2 NA |