题目内容
18.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 2.0gH218O与D216O的混合物中所含中子数为NA | |
| B. | 0.1molCl2溶于足量水中,转移的电子数为0.1NA | |
| C. | 常温常压下50g 46%的乙醇溶液中,所含氧原子数目为0.5NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
分析 A、H218O与D216O的摩尔质量均为20g/mol,且均含10个中子;
B、氯气和水的反应为可逆反应;
C、乙醇溶液中除了乙醇外,水也含氧原子;
D、溶液体积不明确.
解答 解:A、H218O与D216O的摩尔质量均为20g/mol,故2g混合物的物质的量为0.1mol,且两者均含10个中子,故0.1mol混合物中含NA个中子,故A正确;
B、氯气和水的反应为可逆反应,不能进行彻底,故转移的电子数小于0.1NA个,故B错误;
C、乙醇溶液中除了乙醇外,水也含氧原子,故溶液中含有的氧原子的个数大于0.5NA个,故C错误;
D、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
8.下列实验操作能达到实验目的是( )
| A. | 向容量瓶中注入液体时,奖容量瓶的玻璃塞倒置在桌面上防止被污染 | |
| B. | 鉴别NO2和溴蒸汽时,将二者分别通到湿润的KI-淀粉试纸上观察颜色变化 | |
| C. | 将甲烷和乙烯的混合气体通入足量溴水,以除去乙烯 | |
| D. | 将洗净的滴定管放到烘箱中烘干,以加快干燥速度 |
9.在元素周期表的主族元素中,甲元素与乙、丙、丁三种元素上下紧密相邻或左右紧密相邻,丙元素的原子序数等于甲、乙两种元素的原子序数之和,四种元素原子的最外层电子数之和为20.下列说法正确的是( )
| A. | 甲、乙、丙、丁四种元素均为短周期元素 | |
| B. | 元素丁形成的化合物比元素乙形成的化合物少 | |
| C. | 气态氢化物的稳定性比较:甲>乙 | |
| D. | 最高价氧化物对应水化物的酸性比较:甲<丙 |
6.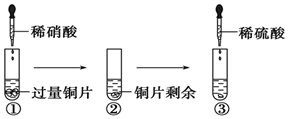 某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是
某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是
( )
 某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是
某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示.下列有关说法正确的是( )
| A. | ①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO2 | |
| B. | ③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O | |
| C. | ③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强 | |
| D. | 由上述实验可知:Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应 |
13.锌一空气燃料电池可作电动车动力电源,电解质溶液为KOH,反应为2Zn+O2+2H2O+4OH-=2Zn(OH)42-.下列说法正确的是( )
| A. | 放电时,电解质溶液中K+移向负极 | |
| B. | 放电时,电解质溶液的pH 不变 | |
| C. | 充电时,阴极的反应为:Zn(OH)42-+2e-=Zn+4OH- | |
| D. | 充电时,当有4.48L 氧气(标准状况下)释放出来时,则析出固体Zn为13g |
10.下列离子方程式书写正确的是( )
| A. | NH4HCO3溶液与过量NaOH溶液反应 NH4++OH-=NH3↑+H2O | |
| B. | 过量CO2通入Ca(ClO)2溶液中 ClO-+CO2+H2O=HCO3-+HClO | |
| C. | 向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+=CO2↑+H2O | |
| D. | 向Ba(OH)2溶液中加入少量NaHSO3溶液 2HSO3-+Ba2++2OH-=BaSO3↓+SO32-+2H2O |
7.下列有关说法正确的是( )
| A. | 加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | |
| B. | 向某溶液中滴加硝酸酸化的BaCl2溶液产生白色沉淀,则该溶液中含有SO42- | |
| C. | 在电解精炼铜过程中,阳极质量的减少多于阴极质量的增加 | |
| D. | 298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其△H<0 |
8.下列说法正确的是( )
| A. | H2O与D2O互为同位素 | B. | 纤维素与淀粉互为同分异构体 | ||
| C. | 干冰和冰为同一种物质 | D. | 甲烷和十六烷互为同系物 |
 .
. .
.