题目内容
用滴定法测定制得的Ce(OH)4产品纯度.

(1)滴定时所用定量仪器的最小刻度为 ;所用FeSO4溶液在空气中露置一段时间后再进进行滴定,则测得该Ce(OH)4产品的质量分数 .(填“偏大”、“偏小”或“无影响”)
(2)称取14.00g硫酸铁铵样品,将其溶于水配制成100mL溶液,分成两等份,向其中一份加入足量NaOH溶液,过滤洗涤沉淀并烘干灼烧至恒重得到1.60g固体;向另一份溶液中加入0.5mol/L Ba(NO3)2溶液100mL,恰好完全反应.则该硫酸铁铵的化学式为 .

(1)滴定时所用定量仪器的最小刻度为
(2)称取14.00g硫酸铁铵样品,将其溶于水配制成100mL溶液,分成两等份,向其中一份加入足量NaOH溶液,过滤洗涤沉淀并烘干灼烧至恒重得到1.60g固体;向另一份溶液中加入0.5mol/L Ba(NO3)2溶液100mL,恰好完全反应.则该硫酸铁铵的化学式为
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)滴定时所用定量仪器的最小刻度为0.1ml,FeSO4溶液在空气中露置一段时间后会被氧化,消耗硫酸亚铁增大;
(2)依据铁元素守恒计算氢氧化铁物质的量,依据硫酸根离子守恒和足量守恒计算分析化学式.
(2)依据铁元素守恒计算氢氧化铁物质的量,依据硫酸根离子守恒和足量守恒计算分析化学式.
解答:
解:(1)滴定时所用定量仪器的最小刻度为0.1mL,估读0.01mL,FeSO4溶液在空气中露置一段时间后会被氧化,消耗硫酸亚铁增大,测定该Ce(OH)4产品的质量分数会偏大;
故答案为:0.1mL;偏大;
(2)称取14.00g样品,将其溶于水配置成100mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到沉淀并烘干灼烧至恒重得到1.60g固体为氧化铁,n(Fe2O3)
=0.01mol,生成氢氧化铁沉淀物质的量为,n(Fe(OH)3)=0.02mol,
向另一份溶液中加入0.05mol Ba(NO3)2溶液,恰好完全反应,则n(SO42-)=0.05mol,
所以14.00g样品中含有Fe2(SO4)30.02mol,n(SO42-)为0.1mol,则(NH4)2SO4为0.1mol-0.02mol×3=0.04mol,
则m(H2O)=14.00g-0.02mol×400g/mol-0.04mol×132g/mol=0.72g,
n(H2O)=
=0.04mol,
n(Fe2(SO4)3):n((NH4)2SO4):n(H2O)=0.02:0.04:0.04=1:2:2,
所以化学式为Fe2(SO4)3?2(NH4)2SO4?2H2O,
故答案为:Fe2(SO4)3?2(NH4)2SO4?2H2O.
故答案为:0.1mL;偏大;
(2)称取14.00g样品,将其溶于水配置成100mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到沉淀并烘干灼烧至恒重得到1.60g固体为氧化铁,n(Fe2O3)
| 1.6g |
| 160g/mol |
向另一份溶液中加入0.05mol Ba(NO3)2溶液,恰好完全反应,则n(SO42-)=0.05mol,
所以14.00g样品中含有Fe2(SO4)30.02mol,n(SO42-)为0.1mol,则(NH4)2SO4为0.1mol-0.02mol×3=0.04mol,
则m(H2O)=14.00g-0.02mol×400g/mol-0.04mol×132g/mol=0.72g,
n(H2O)=
| 0.72g |
| 18g/mol |
n(Fe2(SO4)3):n((NH4)2SO4):n(H2O)=0.02:0.04:0.04=1:2:2,
所以化学式为Fe2(SO4)3?2(NH4)2SO4?2H2O,
故答案为:Fe2(SO4)3?2(NH4)2SO4?2H2O.
点评:本题考查了化学实验基本操作、元素及化合物知识反应等相关知识,提纯制备,为高考常见题型,侧重于学生的分析能力、实验能力和计算能力的考查,注意把握实验的原理和操作方法,题目难度中等.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A、NaCl晶体、BaSO4 |
| B、液态的醋酸、酒精 |
| C、铜、二氧化硫 |
| D、熔融的KNO3、硫酸溶液 |
某元素R的阴离子R2-核外共有a个电子,核内有b个中子,则下列表示R原子的符号中,正确的是( )
| A、abR |
| B、a+ba+2R |
| C、a+b-2a+2R |
| D、a+b-2a-2R |
下列离子方程式正确的是( )
| A、向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-═AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| C、在碳酸氢镁溶液中加入过量氢氧化钠溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| D、向NH4HCO3溶液中加过量的NaOH溶液并加热NH4++OH-═△NH3↑+H2O |
下列说法正确的是( )
| A、2p和3p轨道形状均为哑铃形,能量也相等 |
| B、M层有3个能级,9个轨道 |
| C、第四周期最外层电子数为1,且内层电子全部排满的原子是钾原子 |
| D、在离核最近区域内运动的电子能量最高 |
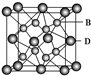 有A、B、C、D、E五种元素,其相关信息如下:
有A、B、C、D、E五种元素,其相关信息如下: