题目内容
19.某样品中含有碳酸铵和碳酸氢铵,取12.7g样品置于锥形瓶中,加人足量的氢氧化钠溶液,加热反应后的溶液,产生的气体经过装有碱石灰的干燥管,最后收集到标准状况下4.48L气体.(1)计算12.7g样品中碳酸氢铵的物质的量.
(2)计算12.7g样品中氮元素的百分含量.
分析 (1)碳酸铵和碳酸氢铵加人足量的氢氧化钠反应方程式为2NaOH+(NH4)2CO3═2NH3↑+2H2O+Na2CO3,2NaOH+NH4HCO3═NH3↑+2H2O+Na2CO3,设碳酸铵和碳酸氢铵的物质的量分别为xmol和与ymol,则96x+79y=12.7①,根据氮原子守恒2x+y=$\frac{4.48}{22.4}$②,解x,y据此进行分析;
(2)w=$\frac{m(N)}{m}×100%$,据此进行计算.
解答 解:(1)碳酸铵和碳酸氢铵加人足量的氢氧化钠反应方程式为2NaOH+(NH4)2CO3═2NH3↑+2H2O+Na2CO3,2NaOH+NH4HCO3═NH3↑+2H2O+Na2CO3,设碳酸铵和碳酸氢铵的物质的量分别为xmol和与ymol,则96x+79y=12.7①,根据氮原子守恒2x+y=$\frac{4.48}{22.4}$②,解得x=0.05mol,y=0.01mol,故n((NH4)2CO3)=0.05mol,n(NH4HCO3)=0.1mol,
答:12.7g样品中碳酸氢铵的物质的量为0.1mol;
(2)m(N)=n(N)M=(0.05mol×2+0.1mol)×14g/mol=2.8g,
w=$\frac{m(N)}{m}×100%$=$\frac{2.8g}{12.7g}×100%$=22.05%,
答:12.7g样品中氮元素的百分含量为22.05%.
点评 本题属于混合物的计算,注意元素守恒在计算过程中的应用,本题题目难度中等.

练习册系列答案
相关题目
4.下列互为同位素的是( )
| A. | Na 和 Na+ | B. | H2和 D2 | C. | 16O 和 18O | D. | CO 和 CO2 |
5.某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做如下探究实验.

已知:①无水氯化铁在空气中易潮解,加热易升华;②工业上,向500-600℃的铁屑中通入氯气和生产无水氯化铁;③向炽热的铁屑中通入氯化氢可以生成无水氯化亚铁和氢气.
(1)仪器N的名称是分液漏斗,N中盛有浓盐酸,烧瓶M中的固体试剂KMnO4(或KClO3)(填化学式).
(2)装置的连接顺序为a→g→h→d→e→b→c→d→e→f.(用小写字母表示,部分装置可重复使用)
(3)若缺少装置E、则对本实验造成的影响是HCl和Fe反应生成的H2与Cl2混合受热发生爆炸,且有杂质氯化亚铁生成;请简述检验产物是否受影响的方法及实验现象:取少量产物于一洁净的试管种加少量水将产物溶解,向其中滴加铁氰化钾溶液,若产生蓝色沉淀,则证明存在氯化亚铁.
(4)已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氧剂,反应后Na2S2O3被氧化为Na2SO4,则装置D中发生反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+
(5)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
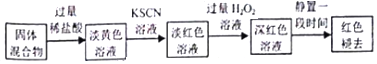
①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是2Fe2++2H++H2O2=2F3++2H2O(用离子方程式表示).
②已知红色褪去的同时有气体产生,经检验气体为O2,该小组对红色褪去的原因进行探究.
由实验Ⅰ和Ⅱ可得出的结论为H2O2将SCN-氧化成SO42-.

已知:①无水氯化铁在空气中易潮解,加热易升华;②工业上,向500-600℃的铁屑中通入氯气和生产无水氯化铁;③向炽热的铁屑中通入氯化氢可以生成无水氯化亚铁和氢气.
(1)仪器N的名称是分液漏斗,N中盛有浓盐酸,烧瓶M中的固体试剂KMnO4(或KClO3)(填化学式).
(2)装置的连接顺序为a→g→h→d→e→b→c→d→e→f.(用小写字母表示,部分装置可重复使用)
(3)若缺少装置E、则对本实验造成的影响是HCl和Fe反应生成的H2与Cl2混合受热发生爆炸,且有杂质氯化亚铁生成;请简述检验产物是否受影响的方法及实验现象:取少量产物于一洁净的试管种加少量水将产物溶解,向其中滴加铁氰化钾溶液,若产生蓝色沉淀,则证明存在氯化亚铁.
(4)已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氧剂,反应后Na2S2O3被氧化为Na2SO4,则装置D中发生反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+
(5)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是2Fe2++2H++H2O2=2F3++2H2O(用离子方程式表示).
②已知红色褪去的同时有气体产生,经检验气体为O2,该小组对红色褪去的原因进行探究.
| 实验 | 操作 | 现象 | |
| 实验Ⅰ (取褪色后溶液3等份) | 第1份 | 滴加FeCl2溶液 | 无明显变化 |
| 第2份 | 滴加KSCN溶液 | 溶液出现红色 | |
| 第3份 | 滴加稀盐酸和BaCl2溶液 | 产生白色沉淀 | |
| 实验Ⅱ (取与褪色后的溶液同浓度的FeCl3溶液) | 滴加2滴KSCN溶液,溶液变红,再通入O2 | 无明显变化 | |
14.若$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-92.3kJ/mol,则HCl(g)═$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)的△H为( )
| A. | +184.6 kJ/mol | B. | -92.3 kJ/mol | C. | -369.2 kJ/mol | D. | +92.3 kJ/mol |
4.写出下列反应的热化学方程式:
(1)3mol NO2(g)与1mol H2O(l)反应生成HNO3(aq)和NO(g),放热138kJ.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)△H=-138kJ/mol;
(2)用CO还原1mol Fe2O3,放热24.8kJ.3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H=-24.8kJ/mol;
(3)1mol HgO(s)分解为液态汞和氧气,吸热90.7kJ.HgO(s)=Hg(l)+$\frac{1}{2}$O2(g)△H=+90.7kJ/mol;
(4)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol;
(5)6.4g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(l)△H=-1135kJ/mol;
(6)已知反应N2+3H2?2NH3△H=a kJ•mol-1.试根据下表中所列键能数据估算a的数值为-93;
(7)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g )+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变△H=+226.7kJ•mol-1.
(1)3mol NO2(g)与1mol H2O(l)反应生成HNO3(aq)和NO(g),放热138kJ.3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)△H=-138kJ/mol;
(2)用CO还原1mol Fe2O3,放热24.8kJ.3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H=-24.8kJ/mol;
(3)1mol HgO(s)分解为液态汞和氧气,吸热90.7kJ.HgO(s)=Hg(l)+$\frac{1}{2}$O2(g)△H=+90.7kJ/mol;
(4)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol;
(5)6.4g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式2CH3OH(1)+3O2(g)═2CO2(g)+4H2O(l)△H=-1135kJ/mol;
(6)已知反应N2+3H2?2NH3△H=a kJ•mol-1.试根据下表中所列键能数据估算a的数值为-93;
| 化学键 | H-H | N-H | N≡N |
| 键能kJ/mol | 436 | 391 | 945 |
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g )+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变△H=+226.7kJ•mol-1.
8.某无色水溶液可能含有以下离子中的若干种:NH4+、Cl-、Fe2+、Ba2+、K+、CO32-、SO42-,现取三份100mL 的该溶液进行如下实验:①第一份加入AgNO3溶液有沉淀产生;②第二份加足量NaOH溶液加热后,收集到气体0.04mol; ③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,用足量盐酸洗涤、干燥后,剩余沉淀质量为2.33g.根据上述实验结果推测以下说法不正确的是( )
| A. | K+一定存在 | B. | 溶液中CO32-浓度为0.1 mol/L | ||
| C. | Cl-可能存在 | D. | Ba2+一定不存在 |
9.下列过程发生化学变化的是( )
| A. | 香水挥发 | B. | 海水晒盐 | ||
| C. | 冷、浓硝酸使铁片钝化 | D. | 干冰升华 |