题目内容
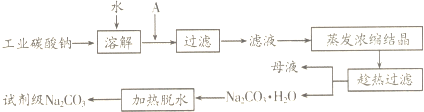
11.三聚氰胺(化学式:C3N6H6)是一种非食品类的重要有机化工原料、广泛用于塑料、造纸、建材等行业.如图是我国科技工作者研制的以尿素为原料生产三聚氰胺的工艺----“常压气相一步法联产纯碱新技术”:已知:①尿素的熔点是132.7℃,常压下超过160℃即可分解;
②三聚氰胺的熔点是354℃,加热易升华,微溶于水;
③以尿素为原料生产三聚氰胺的原理是:6CO(NH2)2$\stackrel{一定条件下}{→}$C3N6H6+6NH3+3CO2
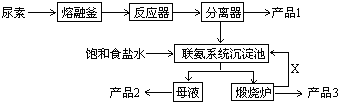
请回答:
(1)尿素是一种常用含氮量最高的化肥,其氮元素的质量百分数为46.67%,在实验室使其熔化的容器名称叫坩埚.
(2)写出各主要成份的化学式:产品2NH4Cl、XCO2;
(3)联氨系统沉淀池中发生的化学反应方程式为CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3.
(4)工业上合成尿素的化学反应方程式为CO2+2NH3→CO(NH2)2+H2O(反应条件可以不写).
(5)为了使母液中析出更多的产品2,常用的方法是A、D
A.加入固体NaCl B.加入固体NaHCO3 C.通入CO2气体 D.通入NH3
(6)若生产过程中有4%的尿素损耗,每吨尿素可生产三聚氰胺0.336吨.(精确到0.001)
分析 (1)根据尿素的分子式CO(NH2)2计算出氮元素的质量分数;实验室熔化尿素需要在坩埚中进行;
(2)根据生产流程分析;
(3)联氨系统沉淀池中,加入饱和食盐水和二氧化碳,大大降低了碳酸氢钠的溶解度,析出碳酸氢钠晶体;
(4)工业上用二氧化碳和氨气反应来制取尿素;
(5)根据方程式判断;
(6)设出三聚氰胺的质量,然后根据反应原理计算出三聚氰胺的质量.
解答 解:(1)尿素的分子式CO(NH2)2,氮元素的质量分数为:$\frac{14×2}{60}$×100%=46.67%;在实验室熔化尿素需要在坩埚中进行;
故答案为:46.67%;坩埚;
(2)根据生产流程,分离器中分离出产品1三聚氰胺;联氨系统沉淀池中加入饱和食盐水和二氧化碳,析出碳酸氢钠晶体,母液主要是氯化铵溶液,利用母液得到产品2氯化铵;X是能够循环利用的二氧化碳;
故答案为:NH4Cl;CO2;
(3)由于联氨系统沉淀池中,加入饱和食盐水和二氧化碳,大大降低了碳酸氢钠的溶度积,析出碳酸氢钠晶体,所以联氨系统沉淀池中发生的化学反应方程式为:CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3;
故答案为:CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3;
(4)工业上合成尿素的化学反应方程式为:CO2+2NH3→CO(NH2)2+H2O,
故答案为:CO2+2NH3→CO(NH2)2+H2O;
(5)根据反应CO2+NH3+NaCl+H2O→NH4Cl+NaHCO3,要从母液中析出更多的碳酸氢钠,可以向溶液中加入氯化钠或者通入二氧化碳气体;
故选A、D;
(6)设生成x吨三聚氰胺,根据方程:
6CO(NH2)2$\stackrel{一定条件下}{→}$C3N6H6+6NH3+3CO2
6×60 126
1t(1-4%) x
则有:360x=(1-4%)×126t,解得x=0.336t;
故答案为:0.336
点评 本题考查了工业流程,涉及的知识点较多、综合性较强,考查同学们灵活运用所学知识进行分析问题、解决问题的能力.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案| A. | 电解AlCl3饱和溶液,可制得金属铝 | |
| B. | 铝热反应不仅被用于焊接钢轨,而且还常被用于冶炼熔点较高的金属 | |
| C. | 铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀 | |
| D. | Al2O3、MgO的熔点很高,可用于制作耐高温材料 |
| A. | 相同温度时,两种饱和溶液中:c(Cl-)≈1.9c(Br-) | |
| B. | AgCl、AgBr组成的混合溶液中:c(Cl-)>c(Br-) | |
| C. | 向饱和AgCl溶液中通入HCl后有沉淀生成,但溶液中c(Cl-)增大 | |
| D. | AgBr在水中溶解度及Ksp均比在NaBr溶液中的大 |