题目内容
8.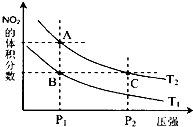 对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是bc.
对反应N2O4(g)?2NO2(g)△H>0,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示,下列说法正确的是bc.a.B、C两点的反应速率:B>C b.由状态B到状态A,可以用加热的方法
c.C点颜色比A点深 d.A、C两点的化学平衡常数:A>C.
分析 N2O4(g)═2NO2(g)△H=+57kJ•mol-1,该反应为吸热反应,升高温度,化学平衡正向移动,NO2的体积分数增大;增大压强,化学平衡逆向移动,NO2的体积分数减小,结合图象来分析解答.
a、B、C两点相比,压强越大,反应速率越快;
b、压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大,A点NO2的体积分数大;
c、增大压强平衡向逆反应进行,向逆反应进行是减小由于压强增大导致浓度增大趋势,但到达平衡仍比原平衡浓度大;
D、A、C点是等温线上的两点,温度不变平衡常数不变.
解答 解:a.由图象可知,B、C两点中,C的压强大,则B、C两点的反应速率:B<C,故A错误;
b.升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,故b正确;
c.由图象可知,A、C两点都在等温线上,C的压强大,与A相比C点平衡向逆反应进行,向逆反应进行是由于减小体积增大压强,平衡移动的结果降低NO2浓度增大趋势,但到达平衡仍比原平衡浓度大,平衡时NO2浓度比A的浓度高,NO2为红棕色气体,则A、C两点气体的颜色:A浅,C深,故c正确;
d.由图象可知,A、C两点都在等温线上,稳定相同则AC点的平衡常数相同,A=C,故d错误;
故选bc.
点评 本题考查化学平衡的图象,明确外界条件对化学平衡的影响及图象中纵横坐标的含义、“定一议二”“先拐先平”原则即可解答,题目难度中等.注意c选项为易错点,改变压强的本质为体积变化.

练习册系列答案
相关题目
13.下列物质的用途叙述错误的是( )
| A. | 硅是制造太阳能电池的常用材料 | |
| B. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 | |
| C. | Na2O2可用作呼吸面具中的供氧剂 | |
| D. | 二氧化硅是制造光导纤维的材料 |
10.在下列化学反应:①H++OH-═H2O;②2H2+O2═2H2O;③HCl+NH3═NH4Cl;④BaCl2+(NH4)2SO4═BaSO4↓+2NH4Cl;⑤Fe+Cu2+═Cu+Fe2+;⑥NaNH2+H2O═NaOH+NH3中,反应时不形成配位键的是( )
| A. | ①②④⑤⑥ | B. | ④⑤⑥ | C. | ②④⑤ | D. | ②③ |
3. 为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过反应CCl4+H2?CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.
为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过反应CCl4+H2?CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.
(1)实验1中,10h后反应达到平衡,则从反应开始至达到平衡状态,H2的平均反应速率为
0.06mol•L-1•h-1.在此实验的平衡体系中,再加入0.5mol CCl4和0.5mol HCl,平衡将怎样移动?向右移动 (填“向左移动”、“向右移动”、“不移动”或“无法确定”).
(2)实验2中,x为B(填字母).
A.等于50% B.大于50% C.小于50% D.无法确定
(3)实验3中的y为0.8.
(4)在100℃条件下,能说明反应CCl4+H2?CHCl3+HCl△H<O达到平衡状态的是D(填字母).
A.压强不再变化
B.生成HCl的速率和消耗H2的速率相等
C.混合气体的密度不变
D.H2的质量不再变化
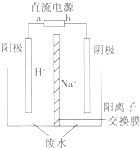
(5)用电解法处理高浓度重铬酸钠废水具有效果稳定可靠,操作管理
简单,设备占地面积小,废水中的重金属离子也能通过电解有所降
低等优点,其原理是铁作电极,在酸性条件下,将Cr6+还原为Cr3+,
其装置示意图如图所示.
①若以甲醚燃料电池为直流电源(电解质溶液为KOH溶液),则燃料电池中b极应通入甲醚,a极的电极反应为13O2+52e-=26O2-.
②能否用铜作电解重铬酸钠废水的电极?不能(填“能”或“不能”),理由是铜做阳极时铜失电子为铜离子,铜离子不能与+6价铬发生氧化还原反应反应得到+3价铬
③除去重铬酸根离子的离子反应是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
 为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过反应CCl4+H2?CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.
为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过反应CCl4+H2?CHCl3+HCl△H<O,使CCl4转化为重要的化工原料氯仿(CHCl3).已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据.| 实验序号 | 温度℃ | 初始CCl4浓度(mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | x |
| 3 | 110 | 0.8 | y | 60% |
0.06mol•L-1•h-1.在此实验的平衡体系中,再加入0.5mol CCl4和0.5mol HCl,平衡将怎样移动?向右移动 (填“向左移动”、“向右移动”、“不移动”或“无法确定”).
(2)实验2中,x为B(填字母).
A.等于50% B.大于50% C.小于50% D.无法确定
(3)实验3中的y为0.8.
(4)在100℃条件下,能说明反应CCl4+H2?CHCl3+HCl△H<O达到平衡状态的是D(填字母).
A.压强不再变化
B.生成HCl的速率和消耗H2的速率相等
C.混合气体的密度不变
D.H2的质量不再变化
(5)用电解法处理高浓度重铬酸钠废水具有效果稳定可靠,操作管理
简单,设备占地面积小,废水中的重金属离子也能通过电解有所降
低等优点,其原理是铁作电极,在酸性条件下,将Cr6+还原为Cr3+,
其装置示意图如图所示.
①若以甲醚燃料电池为直流电源(电解质溶液为KOH溶液),则燃料电池中b极应通入甲醚,a极的电极反应为13O2+52e-=26O2-.
②能否用铜作电解重铬酸钠废水的电极?不能(填“能”或“不能”),理由是铜做阳极时铜失电子为铜离子,铜离子不能与+6价铬发生氧化还原反应反应得到+3价铬
③除去重铬酸根离子的离子反应是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
13.T1℃时,在容积固定的2L密闭容器中,X(g)与Y(g)反应生成Z(g)的物质的量的变化如图甲所示;若保持其它条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图乙所示.则下列结论正确的是( )
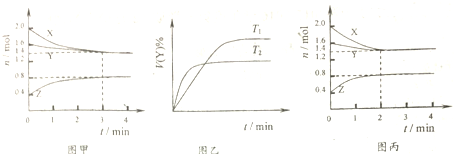

| A. | T1℃时,容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g),且正反应放热 | |
| B. | T1℃时,反应进行的前3min内,用X表示的反应速率v(X)=0.2mol•(L•min)-1 | |
| C. | T1℃时,3min达到平衡后,向容器中再加入2.0mol X、1.6mol Y、0.4mol Z,反应达到新平衡时:0.7mol•L-1<c(Y)<1.4mol•L-1 | |
| D. | 若改变反应条件,使反应进程如图丙所示,则改变的条件是使用催化剂 |
20.下列有关物质的分类或归类正确的是
①混合物:漂白粉、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物:丙烷、异丁烷、十六烷
⑤同素异形体:H2、D2、T2( )
①混合物:漂白粉、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物:丙烷、异丁烷、十六烷
⑤同素异形体:H2、D2、T2( )
| A. | ①③④ | B. | ③④ | C. | ②③④ | D. | ②④ |
17.氯气用于自来水的杀菌消毒,但在消毒时会产生一些负面影响,因此人们开始研究一些新型自来水消毒剂.某学习小组查阅资料发现NCl3可作为杀菌消毒剂,该小组利用下图所示的装置制备NCl3,并探究NCl3的漂白性.NCl3的相关性质如下:
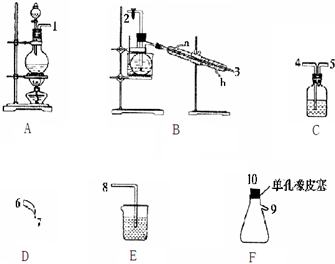
回答下列问题:
(1)根据实验目的,接口连接的顺序为1、4、5、2、3、6、7、10、9、8.
(2)C装置中盛放的试剂为饱和食盐水; E装置中盛放的试剂为NaOH溶液.
(3)A装置中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)B装置中发生反应的化学方程式为3Cl2+NH4Cl═NCl3+4HCl,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为71~95℃.
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,写出该油状液体与热水反应的化学方程式NCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$3HClO+NH3_.
| 物理性质 | 制备原理 | 化学性质 |
| 黄色油状液体 熔点为-40℃,沸点为71℃ 不溶于冷水,易溶于有机溶剂 密度为1.65g/mL | Cl2与NH4Cl水溶液在低温下反应 | 95℃爆炸,热水中发生水解 |

回答下列问题:
(1)根据实验目的,接口连接的顺序为1、4、5、2、3、6、7、10、9、8.
(2)C装置中盛放的试剂为饱和食盐水; E装置中盛放的试剂为NaOH溶液.
(3)A装置中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(4)B装置中发生反应的化学方程式为3Cl2+NH4Cl═NCl3+4HCl,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为71~95℃.
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,写出该油状液体与热水反应的化学方程式NCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$3HClO+NH3_.
18.将一小粒金属钠投入到盛有无水乙醇的小烧杯中,以下描述合理的是( )
| A. | 不反应 | B. | 烧杯内溶液颜色逐渐变红 | ||
| C. | 金属钠沉入烧杯底部,并产生气泡 | D. | 金属钠浮于液面上,四处游动 |