题目内容
12.有A、B、C、D、E 五种元素,它们的核电荷数依次增大,且都小于20.其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1.B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题:(1)以上这五种元素中,属于S区的是H、K(填元素符号).
(2)C、D、E四种元素的简单离子按半径由小到大的顺序为(用离子符号表示)Al3+<K+<S2-.
(3)写出D元素基态原子的外围电子排布式Al3+<K+<S2-.
(4)元素电负性为B>D,元素第一电离能为C>E.(填“>”、“<”或“﹦”)
(5)由这五种元素组成的一种化合物是KAl(SO4)2•12H2O(写化学式).
分析 A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D处于同主族,它们原子最外层的p能级电子数是s能级电子数的两倍,外围电子排布为ns2np4,故B为O元素、D为S元素;C原子最外层上电子数等于D原子最外层上电子数的一半,最外层电子数为3,且为金属元素,故C为Al;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,A为非金属,结合原子序数可知,A为H元素、E为K元素,据此进行解答.
解答 解:A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20,B和D处于同主族,它们原子最外层的p能级电子数是s能级电子数的两倍,外围电子排布为ns2np4,故B为O元素、D为S元素;C原子最外层上电子数等于D原子最外层上电子数的一半,最外层电子数为3,且为金属元素,故C为Al;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,A为非金属,结合原子序数可知,A为H元素,E为K元素,
(1)以上这五种元素中,属于S区的是H、K,
故答案为:H、K;
(2)C为Al,D为S,E为K,离子的电子层越多,离子半径越大,电子层相同时核电荷数越大,离子半径越小,则离子半径大小为:Al3+<K+<S2-,
故答案为:Al3+<K+<S2-;
(3)D为S元素,S原子的最外层含有6个电子,其基态原子的外围电子排布式为:3s23p4,
故答案为:3s23p4;
(4)同主族自上而下电负性减小,故元素电负性为O>S,金属性越强第一电离能越小,故元素第一电离能为Al>K,
故答案为:>;>.
(5)由以上分析可知A为H,B为O,C为Al,D为S,E为K,由这五种元素组成的一种化合物是KAl(SO4)2•12H2O,
故答案为:KAl(SO4)2•12H2O.
点评 本题考查结构位置与性质关系,题目难度中等,推断元素是解题的关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析、理解能力及灵活应用能力.

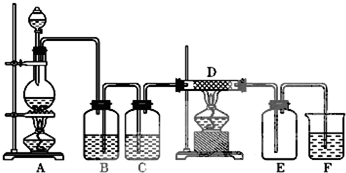
| A. |  装置可干燥、收集并吸收多余的NH3 | |
| B. |  装置除去CO2中含有的少量HCl | |
| C. |  装置可以制备大量的乙炔气体 | |
| D. |  装置不添加任何仪器即可检查气密性 |
| A. | SO2漂白纸浆 | B. | 纯碱清洗油污 | ||
| C. | Na2S除污水中的Cu2+ | D. | 漂白粉漂白织物 |
| A. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| B. | 等物质的量的水与重水含有的中子数 | |
| C. | 同温、同压、同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量盐酸完全反应时转移的电子数 |
| A. | 酸性:H2SO3>H2CO3 | B. | 熔沸点:HF>HCl | ||
| C. | 碱性:NaOH>Al(OH)3 | D. | 热稳定性:Na2CO3>CaCO3 |