题目内容
一定温度下,在容积为2L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示.则下列叙述不正确的是( )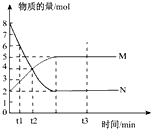

A、化学方程式中
| ||
| B、t2时N 的 v正=v逆. | ||
C、从t1到t2时刻 M的平均反应速率
| ||
| D、t3时混合气体的总物质的量不随时间的变化而变化 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、根据物质的量的变化之比等于化学计量数之比求算;
B、图象分析可知,此点MN物质的量随时间变化而变化,反应正向进行;
C、依据化学反应速率概念计算,v=
计算得到;
D、t3时刻MN物质的量不随时间变化,达到平衡状态.
B、图象分析可知,此点MN物质的量随时间变化而变化,反应正向进行;
C、依据化学反应速率概念计算,v=
| △c |
| △t |
D、t3时刻MN物质的量不随时间变化,达到平衡状态.
解答:
解:A、图象可知
=
=
=2,故A正确;
B、t2时刻MN物质的量相同,但随时间变化MN物质的量发生变化,说明未达到平衡状态,正逆反应速率不等,故B错误;
C、从t1到t2时刻 M的平均反应速率=
=
mol/(L.min),故C正确;
D、t3时反应达到平衡状态,混合气体的总物质的量不随时间的变化而变化,故D正确;
故选B.
| a |
| b |
| △n(N) |
| △n(M) |
| (8-2)mol |
| (5-2)mol |
B、t2时刻MN物质的量相同,但随时间变化MN物质的量发生变化,说明未达到平衡状态,正逆反应速率不等,故B错误;
C、从t1到t2时刻 M的平均反应速率=
| ||
| (t2-t1)min |
| 1 |
| 2(t2-t1) |
D、t3时反应达到平衡状态,混合气体的总物质的量不随时间的变化而变化,故D正确;
故选B.
点评:本题考查了化学平衡建立的过程分析,反应速率计算,平衡状态判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
| B、用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |
| C、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
| D、电解精炼铜时,将粗铜作电解池的阴极,纯铜作电解池的阳极 |
同温同压下,下列气体的密度最大的是( )
| A、F2 |
| B、Cl2 |
| C、HCl |
| D、CO2 |
下列离子方程式不正确的是( )
| A、石英与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| B、硅与烧碱溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ |
| C、向小苏打溶液中加入过量的石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、往水玻璃中加入盐酸:2H++SiO32-═H2SiO3↓ |
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C、碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
以下说法不正确的是( )
| A、从元素周期表中可以获取元素名称、原子序数、相对原子质量等信息 |
| B、物质本身没有好与坏之分,而人们对物质的应用却存在合理与不合理之分 |
| C、对于化学变化,根据不同的需求,人们需要控制反应条件促进或抑制反应的发生 |
| D、科学家创建元素符号、化学方程式等化学用语,是为了增加化学科学的神秘色彩 |
下列各组有机物只用一种试剂无法鉴别的是( )
| A、乙醇、乙酸、乙酸乙酯 |
| B、苯酚、己烯、四氯化碳 |
| C、对二甲苯、苯、环己烷 |
| D、乙醛、乙酸、葡萄糖 |