题目内容
13.归纳是学习化学的一种常用方法,某同学归纳的物质及其所属类別与右图的对应关系正确的是( )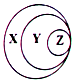
| A. | X-胶体 Y-混合物 Z-淀粉溶液 | B. | X-化合物 Y-含氧酸盐 Z-氯化钠 | ||
| C. | X-气态氢化物 Y-酸 Z-盐酸 | D. | X-强电解质 Y-强酸 Z-硫酸 |
分析 由图可知,概念的范畴为X包含Y,Y包含Z,然后利用物质的组成和性质来分析物质的类别,再根据概念的从属关系来解答.
解答 解:A、混合物不一定是胶体,故A错误;
B、氯化钠不是含氧酸盐,故B错误;
C、酸不一定是气态氢化物,盐酸为氯化氢的水溶液为混合物,故C错误;
D、硫酸是强酸,属于强电解质,关系正确,故D正确.
故选D.
点评 本题考查物质的组成和分类,学生应能识别常见物质的种类,并能利用其组成来判断物质的类别是解答的关键,题目较简单,属于基础题.

练习册系列答案
相关题目
4.足量铁粉与一定量的盐酸反应,为了减慢反应速率,但不减少氢气的产量,可加入下列物质中的( )
| A. | 水 | B. | NaOH固体 | C. | Na2CO3固体 | D. | NaNO3溶液 |
1. 完成下列问题:
完成下列问题:
(1)某学习小组用0.80mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸.
①滴定管如图所示,用甲 (填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸溶液.
②用滴定的方法来测定盐酸的浓度,实验数据如表所示:
该未知盐酸的浓度为0.92mol/L(保留两位有效数字).
(2)若用酚酞作指示剂,达到滴定终点的标志是无色变粉红色且30s不变色.
(3)造成测定结果偏高的操作可能是BC.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的读数时,滴定前仰视凹液面最低处,滴定后俯视读数.
 完成下列问题:
完成下列问题:(1)某学习小组用0.80mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸.
①滴定管如图所示,用甲 (填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸溶液.
②用滴定的方法来测定盐酸的浓度,实验数据如表所示:
| 实验编号 | 待测盐酸溶液的体积/mL | 滴入NaOH溶液的体积/mL |
| 1 | 20.00 | 23.00 |
| 2 | 20.00 | 23.10 |
| 3 | 20.00 | 22.90 |
(2)若用酚酞作指示剂,达到滴定终点的标志是无色变粉红色且30s不变色.
(3)造成测定结果偏高的操作可能是BC.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的读数时,滴定前仰视凹液面最低处,滴定后俯视读数.
8.下列物质中能导电的是( )
| A. | 稀硫酸 | B. | 蔗糖 | C. | CuSO4•5H2O | D. | NaCl固体 |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18 g H2O含有10NA个质子 | |
| B. | 7.8 g Na2O2中含有的阴离子数是0.2NA | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
2.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 15g甲基(-CH3)所含有的电子数是10 NA个 | |
| B. | 标准状况下,2.24 L CHCl3的原子总数为0.5 NA个 | |
| C. | 4.2g C3H6中含有的碳碳双键数一定为0.1NA | |
| D. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 |
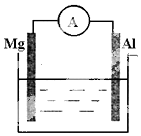 如图所示装置:
如图所示装置: