题目内容
9.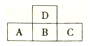 短周期的四种元素位置如图所示,若四种元素的核电荷数之和为52,则与四种元素推断相关的描述不正确的是( )
短周期的四种元素位置如图所示,若四种元素的核电荷数之和为52,则与四种元素推断相关的描述不正确的是( )| A. | A的最高价氧化物用于制作光导纤维 | |
| B. | B的最高价氧化物的水化物是一种强酸 | |
| C. | C至少有两种价态的氧化物 | |
| D. | D的一种单质是空气中含量最多的气体 |
分析 设B的原子序数为x,则D的原子序数为x-8,A的原子序数为x-1,C的原子序数为x+1,则x+x-8+x-1+x+1=52,x=15,则A为Si、B为P、C为O、D为N元素,结合对应的单质、化合物的性质以及元素周期率解答该题.
解答 解:由以上分析可知A为Si、B为P、C为O、D为N元素,
A.A为Si,对应的氧化物为二氧化硅,可用于制作光导纤维,故A正确;
B.B为P,对应的最高价氧化物的水化物是一种中强酸,故B错误;
C.C为O,与钠对应的氧化物有氧化钠、过氧化钠,O元素的化合价为-2、-1价,故C正确;
D.D为N元素,氮气是空气中含量最多的气体,故D正确.
故选B.
点评 本题考查位置、结构、性质的关系及应用,为高考常见题型,题目难度中等,元素的推断是解答本题的关键,并熟悉元素化合物的性质来解答,试题综合性较强,充分考查了学生的灵活应用能力.

练习册系列答案
相关题目
19.某混合物的水溶液中可能含有以下离子中的若干种:Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-,现分别取100mL的两份溶液进行如下实验.
①第一份加过量NaOH溶液后加热,收集到0.01mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到11.65g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
①第一份加过量NaOH溶液后加热,收集到0.01mol气体,无沉淀生成,同时得到溶液甲.
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧后,得到1.02g固体.
③第二份加足量BaCl2溶液后,生成白色沉淀,过滤后的沉淀经足量盐酸洗涤、干燥后,得到11.65g固体,向滤液中加入AgNO3溶液又有白色沉淀产生.下列有关叙述正确的是( )
| A. | 由①可知原溶液存在离子为NH4+,其浓度为0.01mol/L | |
| B. | 原溶液一定存在Cl- | |
| C. | 原溶液肯定没有Fe3+、Mg2+,一定含有Na+ | |
| D. | n(NH4+):n(Al3+):n(SO42-)=1:1:5 |
20.科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O$?_{TiO_{2}}^{激光}$2H2↑+O2↑.制得的氢气可用于燃料电池.
(1)分解海水时,实现了从太阳能转变为化学能.生成的氢气用于燃料电池时,实现化学能转变为电能.
通常把拆开1mol 某化学键所吸收的能量或形成1mol某化学键所放出的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,化学反应的反应热等于反应中断裂旧化学键的之和与反应中形成新化学键的键能之和的差.
(2)估算1mol N和 3mol H结合生成1mol NH3放出热量为45.4KJ.在一定条件下,N2和H2合成NH3,该反应为放热反应(填“放热”或“吸热”),每生成2mol NH3反应的热值为90.8KJ.
(1)分解海水时,实现了从太阳能转变为化学能.生成的氢气用于燃料电池时,实现化学能转变为电能.
通常把拆开1mol 某化学键所吸收的能量或形成1mol某化学键所放出的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,化学反应的反应热等于反应中断裂旧化学键的之和与反应中形成新化学键的键能之和的差.
| 化学键 | H-H | N≡N | N-H |
| 键能/KJ•mol-1 | 436 | 946 | 390.8 |
17.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.根据下表中短周期元素的原子半径和主要化合价,回答表后的问题.
(1)上述元素中与元素⑧处于同一周期的有Mg、P、Cl(填元素符号)
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤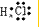 ②⑤
②⑤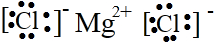 ③⑦
③⑦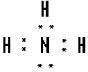
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)元素①在元素周期表中的位置是第二周期ⅥA族
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为H2O>NH3>PH3(填化学式)
(4)请写出下列元素形成的常见化合物的电子式:
③⑤
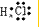 ②⑤
②⑤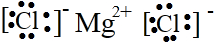 ③⑦
③⑦
(5)请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:3H++Al(OH)3═Al3++3H2O.
4.图为①〜⑥六种烃分子的模型(小黑球代表碳原子,短线代表共价键,氢原子省略)下列说法中不正确的是( )
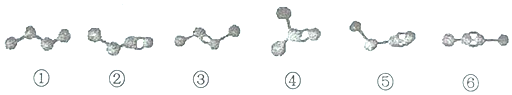

| A. | 烃②、③、④的分子式均为C4H8,三者互为同分异构体 | |
| B. | 烃⑤和⑥的分子式均为C4H6,二者互为同分异构体 | |
| C. | 烃②、③、⑤、⑥分别与足量氧气发生加成反应,均可得到烃① | |
| D. | 等物质的量的烃②和⑤分别在氧气中完全燃烧,烃⑤消耗的氧气多 |
14.下列能够构成原电池的是( )
| A. | 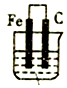 稀硫酸 | B. | 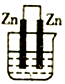 稀盐酸 | C. | 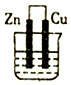 酒精 | D. | 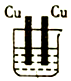 硫酸铜 |
18.无放射性的同位素被称之为“稳定同位素”,在陆地生态系统研究中,2H、13C、15N、18O、34S等常作环境分析指示物.下列有关一些“稳定同位素”的说法错误的是( )
| A. | 34S原子核内中子数为18 | B. | 2H+的酸性比1H+的酸性更强 | ||
| C. | 16O与18O的化学性质几乎完全相同 | D. | 13C和15N原子核内的质子数相差1 |
19. 将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
 将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )| A. | 该物质属于无机物 | |
| B. | 该物质是一种芳香烃 | |
| C. | 该物质不可能使溴水褪色 | |
| D. | 1mol该物质最多可与3molH2发生加成反应 |