题目内容
6.2008年北京奥运会的游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯.下列说法正确的是( )| A. | 聚四氟乙烯有固定的熔点 | |
| B. | 合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应 | |
| C. | 聚全氟乙丙烯分子的结构简式可能为 | |
| D. | ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式 |
分析 A.聚四氟乙烯中n不确定,为混合物;
B.四氟乙烯与乙烯生成ETFE、四氟乙烯与六氟丙烯生成聚全氟乙丙烯都是加聚反应;
C.-CF3-中碳原子超过4个价键;
D.CF2=CF2、CH2=CH2的链节分别为:-CF2-CF2-、-CH2-CH2-.
解答 解:A.聚四氟乙烯中n不确定,为混合物,则无固定熔沸点,故A错误;
B.四氟乙烯和乙烯分子中都含有碳碳双键,二者通过加聚反应生成ETFE;四氟乙烯与六氟丙烯都含有碳碳双键,二者通过加聚反应生成全氟乙丙烯,所以两个反应都是加聚反应,故B正确;
C.结构简式中,-CF3-中碳原子超过4个价键,其链节应该为-CF2-CF2-CF(CF3)-或-CF2-CF2-CF(CF3)-CF2-,故C错误;
D.CF2=CF2、CH2=CH2的链节分别为:-CF2-CF2-、-CH2-CH2-,所以ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式,故D正确;
故选BD.
点评 本题考查有机物的结构与性质,为高频考点,把握加聚反应中高分子与单糖的结构为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
相关题目
16.下列说法中正确的是( )
| A. | 3p2表示3p能级有两个轨道 | |
| B. | 1s22s12p1表示的是激发态原子的电子排布 | |
| C. | M能层中的原子轨道数目为3 | |
| D. | 处于同一轨道上的电子可以有多个,它的运动状态完全相同 |
17.用如图实验装置进行物质的制备,设计正确且能达到实验目的是( )
| A. | 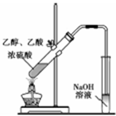 用如图装置制备纯净的乙酸乙酯 | |
| B. | 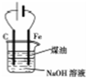 用如图装置制备Fe(OH)2,并能保持一段时间的白色 | |
| C. | 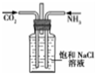 用如图装置先通CO2、在通NH3制备Na2CO3 | |
| D. | 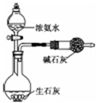 用如图装置制取少量NH3 |
1.下列叙述正确的是( )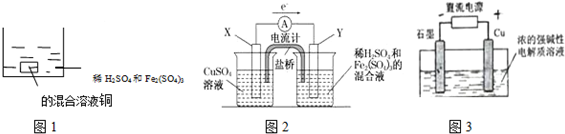

| A. | 如图1 所示将一定量的铜片加入到100 mL 稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO42-)为0.5mol/L | |
| B. | 如图2 所示的装置中发生Cu+2Fe3+═Cu2++2Fe2+的反应,X 极是负极,Y 极的材料名称可以是铜 | |
| C. | Cu2O 是一种半导体材料,基于绿色化学理念设计的制取.Cu2O 的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应 | |
| D. | 如图3 所示当有0.1mol 电子转移时,有0.1molCu2O 生成 |
11.日常生活中遇到的很多问题都涉及化学知识,下列有关叙述不正确的是( )
| A. | Al2O3熔点高,可用作耐高温材料 | |
| B. | 用米汤检验含碘盐中的碘酸钾 | |
| C. | 用纯碱溶液洗涤餐具上的油污 | |
| D. | 利用丁达尔效应区别蛋白质溶液和食盐水 |
18.下列反应中,属于加成反应的是( )
| A. | SO3+H2O=H2SO4 | B. | CH2=CH2+HClO→CH3-CHOH | ||
| C. | CH3Cl+Cl2→CH2Cl2+HCl | D. | CO2+2NaOH=Na2CO3+H2O |
15.下面列举的是某化合物的组成和性质,能说明该物质肯定是有机物的是( )
| A. | 仅由碳、氢两种元素组成 | B. | 仅由碳、氢、氧三种元素组成 | ||
| C. | 在氧气中燃烧只生成二氧化碳 | D. | 熔点低而且难溶于水 |
16.某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备制备氯气,化学方程式为:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O.并对氯气的性质进行探究.
(1)氯气制备:

①欲收集一瓶干燥的氯气,请按接口序号完成“制取→收集”的连接顺序为:
b→c→d→g→h→i→j→k
②制备氯气也可用高锰酸钾固体和浓盐酸在常温下制得,其化学方程式为:
□KMnO4+□HCl(浓)→□MnCl2+□Cl2↑+□KCl+□8H2O
请配平上述化学方程式.
③请写出仪器G中可能反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O
(2)性质检验:将氯气溶于水后,进行实验检测.所用试剂有:0.01mol/LAgNO3溶液、紫色石蕊试液.
(1)氯气制备:

①欲收集一瓶干燥的氯气,请按接口序号完成“制取→收集”的连接顺序为:
b→c→d→g→h→i→j→k
②制备氯气也可用高锰酸钾固体和浓盐酸在常温下制得,其化学方程式为:
□KMnO4+□HCl(浓)→□MnCl2+□Cl2↑+□KCl+□8H2O
请配平上述化学方程式.
③请写出仪器G中可能反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O
(2)性质检验:将氯气溶于水后,进行实验检测.所用试剂有:0.01mol/LAgNO3溶液、紫色石蕊试液.
| 操作步骤 | 实验现象 | 解释原因 |
 | 滴加硝酸银溶液,现象有:产生白色沉淀 | 原因有:氯气与水反应后,电离出Cl-,Cl-与Ag+生成AgCl白色沉淀 |
 | 滴加紫色石蕊试液,现象有:先变红,后褪色 | 原因有:氯气与水反应后,溶液显酸性使紫色石蕊试液变红,产生的HClO又使红色的石蕊试液发生漂白 |