题目内容
4.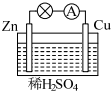 如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )
如图所示是 Zn和 Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )①Cu为负极,Zn为正极;
②Cu极上有气泡产生,发生还原反应;
③SO42-向 Cu极移动;
④若有 0.5mol电子流经导线,则可产生0.25mol气体;
⑤正极反应式:Cu+2e-═Cu2+,发生氧化反应;
⑥电子的流向是:Cu→Zn.
| A. | ①②③ | B. | ②④⑥ | C. | ③④⑤ | D. | ②④ |
分析 Zn-Cu原电池中,Zn作负极,Cu为正极,发生电池反应Zn+2H+=Zn2++H2↑,电子由负极流向正极,阳离子向正极移动,以此来解答.
解答 解:①Zn活泼失电子,则Zn为负极,Cu为正极,故①错误;
②Cu极上氢离子得电子发生还原反应,所以Cu上有气泡产生,故②正确;
③溶液中阴离子向负极移动,即SO42-向 Zn极移动,故③错误;
④Cu为正极,正极电极上发生2H++2e-=H2↑,若有 0.5mol电子流经导线,则可产生0.25mol气体,故④正确;
⑤Cu为正极,正极电极上发生2H++2e-=H2↑,发生还原反应,故⑤错误;
⑥电子由负极流向正极,即电子的流向是:Zn→Cu,故⑥错误;
故选D.
点评 本题考查原电池,明确电极的判断、发生的电极反应、电子、离子的移动方向即可解答,题目难度不大,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列可逆反应平衡常数,其表达式或与有关常数的关系正确的是( )
| A. | 反应C(s)+H2O(g)?CO(g)+H2(g) 的平衡常数为:K=$\frac{c(CO)•c({H}_{2})}{c(C)•c({H}_{2}O)}$ | |
| B. | 反应Cr2O72-+H2O?2CrO42-+2H+ 的平衡常数为:K=$\frac{c(Cr{O}_{4}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{O}_{3}^{2-})•c({H}_{2}O)}$ | |
| C. | NH4++H2O?NH3•H2O+H+的平衡常数为:K=$\frac{{K}_{W}}{{K}_{b}(N{H}_{3}•{H}_{2}O)}$ | |
| D. | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq)的平衡常数为:K=$\frac{{K}_{sp}(A{g}_{2}S)}{{{K}_{sp}}^{2}(AgI)}$ |
15.“2016年地球一小时”推出“为”蓝生活主题,鼓励公众践行可持续的生活和消费方式.下列做法与之不符的是( )
| A. | 利用太阳能制氢 | B. | 用家用汽车代替公交车 | ||
| C. | 利用化石燃料制造燃料电池 | D. | 用节能灯代替白炽灯 |
12.某有机物A由C、H、O三种元素组成,相对分子质量为90.将9.0克A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4克和13.2克.A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物.关于A的说法正确的是( )
| A. | 分子式是C3H8O3 | |
| B. | A催化氧化的产物能发生银镜反应 | |
| C. | 0.1molA与足量Na反应能够产生2.24LH2(标准状况) | |
| D. | A在一定条件下能发生加聚反应 |
19.结构为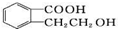 的有机物可以通过不同的反应得到下列四种物质
的有机物可以通过不同的反应得到下列四种物质
①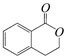 ②
②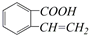 ③
③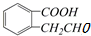 ④
④ ,
,
生成这四种有机物的反应类型依次为( )
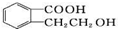 的有机物可以通过不同的反应得到下列四种物质
的有机物可以通过不同的反应得到下列四种物质①
 ②
② ③
③ ④
④ ,
,生成这四种有机物的反应类型依次为( )
| A. | 取代反应、消去反应、酯化反应、加成反应 | |
| B. | 取代反应、消去反应、氧化反应、取代反应 | |
| C. | 酯化反应、取代反应、缩聚反应、取代反应 | |
| D. | 酯化反应、消去反应、取代反应、氧化反应 |
9.下列气体中,对人体无毒害作用的是( )
| A. | Cl2 | B. | N2 | C. | CO | D. | NO2 |
16.在一定条件下,反应2SO2+O2?2SO3在2L密闭容器中进行,5min内SO3的质量增加了16.0g,则该反应的速率为( )
| A. | v(O2)=0.02mol•L-1•min-1 | B. | v(SO3)=0.04mol•L-1•min-1 | ||
| C. | v(SO2)=0.02mol•L-1•min-1 | D. | v(SO3)=0.01mol•L-1•min-1 |

