题目内容
下列离子方程式不正确的是( )
| A、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相混合均匀4AlO2-+7H++H2O=3Al(OH)3↓+Al3+ |
| B、向100mL0.1mol/L的碳酸钠溶液中逐滴加入0.1mol/L CH3COOH:CO32-+CH3COOH=CO2↑+2CH3COO-+H2O |
| C、向硫酸铝铵溶液中滴加过量的氢氧化钡溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| D、KHS的水解:HS-+H2O?H2S+OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.4molNaAlO2和7molHCl反应生成3mol氢氧化铝和1mol氯化铝;
B.碳酸钠与等物质的量的醋酸反应生成碳酸氢钠和醋酸钠;
C.硫酸铝铵溶液中滴加过量的氢氧化钡溶液反应生成硫酸钡、一水合氨和水;
D.KHS的水解生成氢氧化钾和硫化氢.
B.碳酸钠与等物质的量的醋酸反应生成碳酸氢钠和醋酸钠;
C.硫酸铝铵溶液中滴加过量的氢氧化钡溶液反应生成硫酸钡、一水合氨和水;
D.KHS的水解生成氢氧化钾和硫化氢.
解答:
解:A.4molNaAlO2和7molHCl反应的离子方程式:4AlO2-+7H++H2O=3Al(OH)3↓+Al3+,故A正确;
B.碳酸钠与等物质的量的醋酸反应,离子方程式:CO32-+CH3COOH=HCO3-+CH3COO-,故B错误;
C.向硫酸铝铵溶液中滴加过量的氢氧化钡溶液,离子方程式:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O,故C正确;
D.KHS的水解的离子方程式:HS-+H2O?H2S+OH-,故D正确;
故选:B.
B.碳酸钠与等物质的量的醋酸反应,离子方程式:CO32-+CH3COOH=HCO3-+CH3COO-,故B错误;
C.向硫酸铝铵溶液中滴加过量的氢氧化钡溶液,离子方程式:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O,故C正确;
D.KHS的水解的离子方程式:HS-+H2O?H2S+OH-,故D正确;
故选:B.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的化学反应为解答的关键,侧重反应物用量对反应的影响的离子反应考查,题目难度中等.

练习册系列答案
相关题目
往c(H+)相等的一元酸HA和HB的溶液中分别加入适量的锌粉,充分反应后,当收集到的H2气体相等时,消耗酸的体积V(HA)>V(HB),下列分析正确的是( )
| A、消耗锌的质量m(HA)>m(HB) |
| B、HA一定是强酸 |
| C、消耗酸的物质的量n(HA)=n(HB) |
| D、生成H2的平均速率V(HA)<V(HB) |
下列说法正确的是( )
| A、增加水的量或升高温度,可以加快镁跟水的反应速率 |
| B、增大硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率 |
| C、在反应2H++S2O32-=S↓+SO2+H2O中,增大压强,可以加快硫析出的速率 |
| D、煅烧硫铁矿时,把硫铁矿粉碎或通入纯O2可加快反应的速率 |
下列关于命名的说法中错误的是( )
| A、所有烃类的命名都应选择含碳原子最多的链作主链,即“最多”原则 |
| B、二甲苯可以以邻、间、对这种习惯方法进行命名 |
| C、二甲苯也可以用系统方法进行命名 |
| D、化学式是C8H10的苯的同系物有4种同分异构体 |
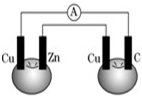 如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )
如图所示,铜片、锌片和石墨棒用导线连接后插入番茄里,电流计中有电流通过,则下列说法正确的是( )| A、锌片是负极 |
| B、两个铜片上都发生氧化反应 |
| C、石墨是阳极 |
| D、两个蕃茄都形成原电池 |
下列实验操作正确的是( )
| A、用托盘天平称量4.00g氢氧化钠固体 |
| B、用10mL量筒量取8.5mL蒸馏水 |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
下列离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | ||
B、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-═2AlO
| ||
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | ||
| D、FeCl2溶液中通入足量的Cl2:Fe2++Cl2═Fe3++2Cl- |
下列说法中,不正确的是( )
| A、相对分子质量相同,组成元素的百分含量相同的不同有机物一定是同分异构体的关系 |
| B、碳原子数相同、结构不同的烷烃一定是互为同分异构体关系 |
| C、两有机物互为同系物,则它们也是互为同分异构体关系 |
| D、碳原子数≤10的烷烃,其一氯代物没有同分异构体的烷烃有4种 |
