题目内容
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:

(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-═Cu2+.
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式).
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 .
(4)写出用SO2还原AuCl4-的离子方程式 .
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 .
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 .

(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有:
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是
(3)操作I的主要步骤为
(4)写出用SO2还原AuCl4-的离子方程式
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,焙烧后金属铜成为氧化铜,酸浸可以得到硫酸铜溶液,硫酸铜溶液经过蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥获得硫酸铜晶体;Au(金)和PbSO4等杂质经王水、浓硝酸氧化后可以得到硝酸铅以及含有AuCl4-+的物质,硝酸铅中加入硫酸可以转化为硫酸铅,AuCl4-可以被SO2还原得到Au.
(1)电解精炼的粗铜作阳极,粗铜中的铜和铅会发生失电子的氧化反应,据此回答;
(2)阳极泥的成分为Cu、Au(金)和PbSO4 等,在焙烧过程中铜被氧化为了CuO,根据阳极泥充分的粉碎,增大接触面积可以提高焙烧效率来回答;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,操作II是从酸浸渣(PbSO4)中得到碱浸渣(PbCO3),据此回答;
(4)SO2还原AuCl4-反应得到氧化产物是SO42-,还原产物是Au,配平书写方程式;
(5)将滤液1并入硫酸铜溶液进行循环操作,有利于充分利用,据此回答;
(6)碳酸铅比硫酸铅更加难溶,往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应.
(1)电解精炼的粗铜作阳极,粗铜中的铜和铅会发生失电子的氧化反应,据此回答;
(2)阳极泥的成分为Cu、Au(金)和PbSO4 等,在焙烧过程中铜被氧化为了CuO,根据阳极泥充分的粉碎,增大接触面积可以提高焙烧效率来回答;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,操作II是从酸浸渣(PbSO4)中得到碱浸渣(PbCO3),据此回答;
(4)SO2还原AuCl4-反应得到氧化产物是SO42-,还原产物是Au,配平书写方程式;
(5)将滤液1并入硫酸铜溶液进行循环操作,有利于充分利用,据此回答;
(6)碳酸铅比硫酸铅更加难溶,往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应.
解答:
解:粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,焙烧后金属铜成为氧化铜,酸浸可以得到硫酸铜溶液,硫酸铜溶液经过蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥获得硫酸铜晶体;Au(金)和PbSO4等杂质经王水、浓硝酸氧化后可以得到硝酸铅以及含有AuCl4-+的物质,硝酸铅中加入硫酸可以转化为硫酸铅,AuCl4-可以被SO2还原得到Au.
(1)电解精炼的粗铜作阳极会发生氧化反应,其中单质铜和活性的金属都会发生溶解,因此粗铜中的铜和铅会发生失电子的氧化反应,电极反应式为:Pb-2e-+SO42-=PbSO4,故答案为:Pb-2e-+SO42-=PbSO4;
(2)由题干可知,用于焙烧的阳极泥的成分为Cu、Au(金)和PbSO4 等,所以在焙烧过程中铜被氧化为了CuO,而Au(金)和PbSO4 均较稳定,要使焙烧效率提高,合理措施是把得到的阳极泥充分的粉碎,增大接触面积,或把反应后的气体在次逆流焙烧,这样可以升高温度且减少能耗,
故答案为:将阳极泥粉碎,逆流焙烧等; CuO;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤,操作II是从酸浸渣(PbSO4)中得到碱浸渣(PbCO3),因此该操作是过滤操作.
故答案为:蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥;过滤;
(4)SO2还原AuCl4-中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au,根据氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,因此得到的反应方程式为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
故答案为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
(5)滤液1是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用,因此类似此处的做法,应该是流程中得到的另一滤液2,此滤液2是在硝酸铅溶液中加入硫酸生成硫酸铅沉淀并过滤走硫酸铅后剩下的溶液,此溶液中H+没有发生反应,因此还有大量的硝酸溶液,所以可以把此滤液当成硝酸加入前面的碱浸渣中溶解碱浸渣,或者与前面碱浸渣步骤需要加入的硝酸合并加以利用,故答案为:用滤液2溶解碱浸渣 (或并入硝酸中);
(6)通过比较两种沉淀的溶度积,可以看出碳酸铅比硫酸铅更加难溶,因此往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应,离子方程式要注意标明状态,方程式为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
故答案为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
(1)电解精炼的粗铜作阳极会发生氧化反应,其中单质铜和活性的金属都会发生溶解,因此粗铜中的铜和铅会发生失电子的氧化反应,电极反应式为:Pb-2e-+SO42-=PbSO4,故答案为:Pb-2e-+SO42-=PbSO4;
(2)由题干可知,用于焙烧的阳极泥的成分为Cu、Au(金)和PbSO4 等,所以在焙烧过程中铜被氧化为了CuO,而Au(金)和PbSO4 均较稳定,要使焙烧效率提高,合理措施是把得到的阳极泥充分的粉碎,增大接触面积,或把反应后的气体在次逆流焙烧,这样可以升高温度且减少能耗,
故答案为:将阳极泥粉碎,逆流焙烧等; CuO;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤,操作II是从酸浸渣(PbSO4)中得到碱浸渣(PbCO3),因此该操作是过滤操作.
故答案为:蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥;过滤;
(4)SO2还原AuCl4-中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au,根据氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,因此得到的反应方程式为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
故答案为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
(5)滤液1是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用,因此类似此处的做法,应该是流程中得到的另一滤液2,此滤液2是在硝酸铅溶液中加入硫酸生成硫酸铅沉淀并过滤走硫酸铅后剩下的溶液,此溶液中H+没有发生反应,因此还有大量的硝酸溶液,所以可以把此滤液当成硝酸加入前面的碱浸渣中溶解碱浸渣,或者与前面碱浸渣步骤需要加入的硝酸合并加以利用,故答案为:用滤液2溶解碱浸渣 (或并入硝酸中);
(6)通过比较两种沉淀的溶度积,可以看出碳酸铅比硫酸铅更加难溶,因此往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应,离子方程式要注意标明状态,方程式为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
故答案为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
点评:本题主要考查学生对物质的分离、离子的检验、粗盐的提纯 等知识的掌握,是一道能力提升题,难度大.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
对于某些离子的检验及结论一定正确的是( )
| A、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加入硝酸银溶液有白色沉淀产生,一定有Cl- |
| D、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:3A(g)+2B(g)?4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A、该反应的化学平衡常数表达式是K=
| ||
| B、此时,B的平衡转化率是35% | ||
| C、增大该体系的压强,平衡向右移动,化学平衡常数 | ||
| D、增加C,B的平衡转化率不变 |
下列依据相关数据作出的推理和判断中,不正确的是( )
| A、依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B、依据溶解度数据,选择用萃取的方法将粗溴提纯 |
| C、依据沸点数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D、依据苯与氢气加成反应的反应热数据与其他烯烃的加成反应对比,研究苯化学键的特征 |
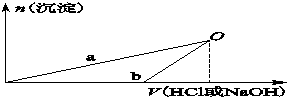 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.方案①:2.7g Al
| 100ml稀盐酸 |
| NaOH溶液 |
方案②:2.7g Al
| 100mlNaOH溶液 |
| 稀盐酸 |
NaOH溶液和稀盐酸的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
| A、X溶液溶质为AlCl3,Y溶液溶质为NaAlO2 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、在O点时两方案中所得溶液浓度相等 |
| D、a、b曲线表示的反应都是氧化还原反应 |
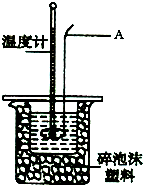 某实验小组用0.50mol?L-1NaOH溶液和0.50mol?L-1.1硫酸溶液进行中和热的测定.
某实验小组用0.50mol?L-1NaOH溶液和0.50mol?L-1.1硫酸溶液进行中和热的测定.