题目内容
17.亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于工业生产的漂白及消毒.下图是过氧化氢法生产亚氯酸钠的工艺流程图:
相关物质的性质如下:
①ClO2沸点低易气化;浓度较高的ClO2气体易分解爆炸.
②NaClO2溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O.

(1)在ClO2发生器中通入SO2的同时鼓入空气,其作用是B(填序号).
A.将SO2氧化成SO3,增强酸性
B.稀释ClO2以防止爆炸
C.将NaClO3氧化成ClO2
(2)160g•L-1 NaOH溶液的物质的量浓度为4 mol/L,在实验室若要配制500mL该物质的量浓度NaOH溶液,应称取NaOH的质量为80克.
(3)在发生器内,NaClO3将与SO2反应生成ClO2.在吸收塔内,ClO2将进一步生成NaClO2.
试写出吸收塔内发生反应的化学方程式:2ClO2+H2O2+2NaOH═2NaClO2+2H2O+O2↑.
(4)从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是B、E、D(填序号).
A.萃取 B.蒸发 C.灼烧 D.过滤 E.冷却结晶.
分析 (1)纯ClO2易分解爆炸,鼓入空气的作用应是稀释ClO2;
(2)浓度g/L表示1L溶液中所含溶质质量的多少.160g/LNaOH溶液表示1L氢氧化钠溶液含有160gNaOH.令溶液体积为1L,计算氢氧化钠的物质的量.利用c=$\frac{n}{V}$计算氢氧化钠溶液的物质的量浓度;
(3)在吸收塔内,ClO2将进一步生成NaClO2.可被过氧化氢氧化;
(4)从溶液中得到含结晶水的晶体,采取蒸发、浓缩、冷却结晶方法.
解答 解:(1)由信息可知,纯ClO2易分解爆炸,发生器中鼓入空气的作用应是稀释ClO2,以防止爆炸,故答案为:B;
(2)160g/LNaOH溶液表示1L氢氧化钠溶液含有160gNaOH.令溶液体积为1L,则160gNaOH的物质的量为$\frac{160g}{40g/mol}$=4mol.所以该溶液氢氧化钠的物质的量浓度c(NaOH)=$\frac{4mol}{1L}$=4mol/L.在实验室若要配制500mL该物质的量浓度NaOH溶液,应称取NaOH的质量为0.5L×160g/L=80.0g,
故答案为:4;80.0;
(3)在吸收塔内,ClO2将进一步生成NaClO2.可被过氧化氢氧化,反应的化学方程式为2ClO2+H2O2+2NaOH═2NaClO2+2H2O+O2↑,
故答案为:2ClO2+H2O2+2NaOH═2NaClO2+2H2O+O2↑;
(4)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体,故答案为:B、E、D.
点评 本题考查物质制备,综合性较强,涉及氧化还原反应、物质分离和提纯的综合应用,明确物质性质及实验基本操作原理是解本题关键,需要学生较强的综合能力,难度较大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
7.NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的CH2Cl2所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 常温常压下,16gO2和O3的混合气体含有的氧原子数为NA | |
| D. | 1molCaC2所含阴离子数为2NA |
8.短周期元素X、Y、Z、W、M的原子序数依次增大,其中X、W同主族,Y+与X2-具有相同的电子层结构;离子半径:W2->M-,Z的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | |
| B. | 原子半径:X>Y>Z | |
| C. | 最高价氧化物对应水化物的酸性:W>Z | |
| D. | 最简单气态氢化物的稳定性:X>W>M |
12.下列关于钠与水反应的说法不正确的是( )
①将一小块钠投入滴有石蕊试液的水中,反应后溶液变蓝
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后按入水中,两者放出的氢气质量相等.
①将一小块钠投入滴有石蕊试液的水中,反应后溶液变蓝
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后按入水中,两者放出的氢气质量相等.
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
2.用激光笔照射某一果冻时,可看到一条光亮的“通路”,说明该果冻属于( )
| A. | 胶体 | B. | 溶液 | C. | 悬浊液 | D. | 乳浊液 |
9.下列离子方程式中,正确的是( )
| A. | 氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+ | |
| B. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| C. | 钠和水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 碳酸氢钠溶液与盐酸反应:CO32-+2H+=CO2↑+H2O |
6.已知常温下浓度为0.1mol•L-1的下列溶液的pH如表所示:
下列有关说法正确的是( )
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 0.1 mol•L-1 Na2CO3溶液中,存在关系:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| B. | 加热0.1 mol•L-1 NaClO溶液测其pH,pH小于9.7 | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以等体积混合,则有c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | 根据上表数据得出三种酸电离平衡常数大小关系为:HF>HClO>H2CO3(一级电离平衡常数) |
7.铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.
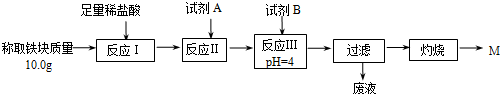
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
①试剂A应选择C,试剂B应选择D.(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
④上述实验应灼烧至M质量不变,则能证明M质量不变的标志是连续两次灼烧质量相差不大于0.1g.
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入足量稀硫酸;观察. | 固体完全溶解,溶液呈黄色. |
继续向上述溶液中滴入几滴(少量)高锰酸钾溶液,振荡观察 | 溶液紫红色未褪去 |
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.
 利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.