题目内容
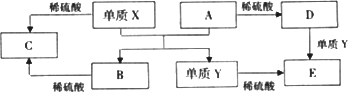
A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如下图所示。
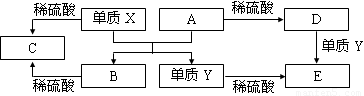
则下列说法正确的是
A.X与A反应的化学方程式是:Al2O3
+ 2Fe Fe2O3 + 2Al
Fe2O3 + 2Al
B.检验D溶液中的金属阳离子的反应:Fe3++3SCN—=Fe(SCN)3↓
C.单质Y在一定条件下能与水发生置换反应
D.由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
【答案】
C
【解析】
试题分析:依据转化关系分析,A+X=B+Y是置换反应。单质X、Y都和稀硫酸反应,说明是金属单质,A、B是氧化物和硫酸反应,其中A和硫酸反应生成的D,D和单质Y反应生成E,说明A中元素化合价是变价,常见的金属是铁元素。综合分析判断,置换反应是铝热反应的置换反应,所以判断X为Al,Y为Fe,A为Fe2O3,B为Al2O3,C为AlCl3,D为FeCl3,E为FeCl2。A、X与A反应的化学方程式是:Fe2O3+2Al Al2O3+2Fe,故A错误;B、检验D溶液中的金属阳离子为三价铁离子发生反应生成的不是沉淀:Fe3++3SCN—=Fe(SCN)3,故B错误;C、单质Y为Fe,在高温条件下能与水蒸汽发生置换反应,生成四氧化三铁和氢气,故C正确;D、由于化合物B为Al2O3既能与酸反应,又能与碱反应,所以是两性化合物,C为AlCl3是盐不具有两性,故D错误,答案选C。
Al2O3+2Fe,故A错误;B、检验D溶液中的金属阳离子为三价铁离子发生反应生成的不是沉淀:Fe3++3SCN—=Fe(SCN)3,故B错误;C、单质Y为Fe,在高温条件下能与水蒸汽发生置换反应,生成四氧化三铁和氢气,故C正确;D、由于化合物B为Al2O3既能与酸反应,又能与碱反应,所以是两性化合物,C为AlCl3是盐不具有两性,故D错误,答案选C。
考点:考查考查无机框图题的判断

练习册系列答案
相关题目

 Fe2O3+2Al
Fe2O3+2Al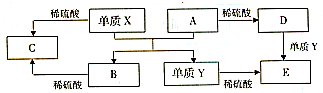

 Fe2O3+2Al
Fe2O3+2Al