��Ŀ����
����Ŀ��������Ԫ��W��X��Y��Z��M��ԭ��������������Ԫ��W��һ�ֺ��ص�������Ϊ0��X��ԭ�������������Ǵ�����2����Z��Mͬ���壬Z2�����Ӳ�ṹ������ͬ��
��1��Mλ��Ԫ�����ڱ��е������壮
��2��������p��W��X��Y��M����Ԫ����ɣ���֪��p��Һ�м���FeCl3��Һ����Һ��Ѫ��ɫ����p��Һ�м���NaOH��Һ�����ȿɷų�ʹʪ��ĺ�ɫʯ����ֽ���������壮p�Ļ�ѧʽΪ ��
��3����X��Y��Z����Ԫ�ؿ����Ħ������Ϊ84gmol��1������q����q����������Ԫ�ص�ԭ�Ӹ���֮��Ϊ1��1��1����֪q�����и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ���ҷ����в���˫�����������Լ��ͷǼ��Լ���q���ӵĽṹʽΪ ��
��4����XY��2��������Cl2���ƣ���XY��2��NaOH��Һ��Ӧ�����ӷ���ʽΪ
��5�������£�1molZ3����Y������⻯�ﷴӦ������һ�ֳ������κ�1molZ2 �� �÷�Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1������VIA
��2��NH4SCN
��3��N��C��O��O��C��N
��4����CN��2+2OH��=CN��+CNO��+H2O
��5��2NH3+4O2=NH4NO3+4O2+H2O
���������⣺Ԫ��W��һ�ֺ��ص�������Ϊ0��ӦΪH��X��ԭ�������������Ǵ�����2����ӦΪCԪ�أ�Z��Mͬ���壬Z2�����Ӳ�ṹ������ͬ����ZΪOԪ�أ�MΪSԪ�أ��ɴ˿�֪YΪNԪ�أ���1��MΪSԪ�أ�λ�����ڱ�����������VIA�����Դ��ǣ�����VIA����2����p��Һ�м���FeCl3��Һ����Һ��Ѫ��ɫ��˵������SCN�����ӣ���p��Һ�м���NaOH��Һ�����ȿɷų�ʹʪ��ĺ�ɫʯ����ֽ���������壬˵������笠����ӣ���ӦΪNH4SCN�����Դ��ǣ�NH4SCN����3��X������Ԫ�ص�ԭ����Ŀ֮��Ϊ1��1��1�������ʽΪ����CON��x �� ��x= ![]() =2�����Է���ʽΪ����CON��2 �� ��ԭ�Ӿ��ﵽ8�����ȶ��ṹ���ҷ�������˫�������ԽṹʽΪ��N��C��O��O��C��N�����Դ��ǣ�N��C��O��O��C��N����4����CN��2��������Cl2���ƣ���CN��2��NaOH��Һ��Ӧ�����ӷ���ʽΪ��CN��2+2OH��=CN��+CNO��+H2O�����Դ��ǣ���CN��2+2OH��=CN��+CNO��+H2O����5�������£�1molO3����N������⻯�ﷴӦ������һ�ֳ������κ�1molN2 �� �÷�Ӧ�Ļ�ѧ����ʽΪ2NH3+4O2=NH4NO3+4O2+H2O��
=2�����Է���ʽΪ����CON��2 �� ��ԭ�Ӿ��ﵽ8�����ȶ��ṹ���ҷ�������˫�������ԽṹʽΪ��N��C��O��O��C��N�����Դ��ǣ�N��C��O��O��C��N����4����CN��2��������Cl2���ƣ���CN��2��NaOH��Һ��Ӧ�����ӷ���ʽΪ��CN��2+2OH��=CN��+CNO��+H2O�����Դ��ǣ���CN��2+2OH��=CN��+CNO��+H2O����5�������£�1molO3����N������⻯�ﷴӦ������һ�ֳ������κ�1molN2 �� �÷�Ӧ�Ļ�ѧ����ʽΪ2NH3+4O2=NH4NO3+4O2+H2O��
���Դ��ǣ�2NH3+4O2=NH4NO3+4O2+H2O��

����Ŀ������ͨѶ�ǹ��ά�����źŵ�һ��ͨѶ�ֶΣ��ϳɹ��ά�������裨һ����Ϳ�㣩�Ĺ���������ͼ�� 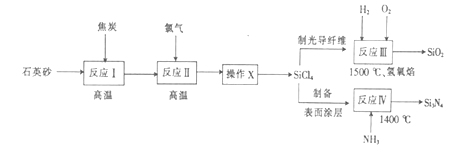
�ش��������⣺
��1����ӦI�Ļ�ѧ����ʽΪ �� ������Ϊ���ѧʽ����
��2������ӦII���õ����Ȼ����Ʒ�����������������
������� | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
�������� | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
�е�/�� | 57.6 | 31.8 | 8.2 | ��85 | 12.5 | 75.5 |
ͼ�С�����X��������Ϊ��PCl3�ĵ���ʽΪ
��3����ӦIII��IV��β������;Ϊ����ӦIV�Ļ�ѧ����ʽΪ ��