题目内容
2.0.1mol某元素的单质一定条件与硫反应后,质量增加3.2g,这种元素是( )| A. | Na | B. | Fe | C. | Cu | D. | Al |
分析 0.1mol某元素的单质一定条件与硫反应后,质量增加3.2g,则增加的3.2g为S的质量,其物质的量为0.1mol,则金属与S按物质的量之比1:1反应.
解答 解:0.1mol某元素的单质一定条件与硫反应后,质量增加3.2g,则增加的3.2g为S的质量,其物质的量为$\frac{3.2g}{32g/mol}$=0.1mol,则金属与S按物质的量之比1:1反应,反应中S表现-2价,则金属表现+2价,而反应中Na为+1价、Fe为+2价、Cu为+1价、Al为+3价,故该元素为Fe,
故选:B.
点评 本题考查化学方程式计算,比较基础,关键是判断金属与硫的化学计量数关系.

练习册系列答案
相关题目
12.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、NO的混合气体,这些气体与3.2g O2混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入NaOH溶液至Cu2+恰好完全沉淀,则消耗溶液中NaOH的质量是( )
| A. | 16 g | B. | 32 g | C. | 64 g | D. | 无法计算 |
13.需加入适当的氧化剂才能实现的反应是( )
| A. | Fe2O3→Fe3O4 | B. | Na2S4→Na2S2 | C. | S2O32-→S4O62- | D. | Cl3-→Cl- |
17.近段时间,我市经常被雾霾笼罩,雾霾天气的形成原因既有气象原因,也有污染排放原因.所以环境保护是我们当今面临的重大课题,下列污染现象主要与氮氧化合物无关的是( )
| A. | 臭氧空洞 | B. | 酸雨 | C. | 光化学烟雾 | D. | 温室效应 |
7.下列有关化学术语或物质变化的说法不正确的是( )
| A. | Na+的结构示意图为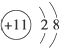 | |
| B. | 明矾的化学式为KAl(SO4)2•12H2O | |
| C. | 某微粒的电子数等于质子数,则该微粒可能是分子或离子 | |
| D. | 化学变化不产生新元素,产生新元素的变化不是化学变化 |