题目内容
25℃的下列溶液中,碱性最强的是( )
| A、pH=11的溶液 |
| B、c(OH-)=0.01mol/L的溶液 |
| C、1L溶液中含有4gNaOH的溶液 |
| D、c(H+)=1×10-10mol/L的溶液 |
考点:pH的简单计算,水的电离
专题:电离平衡与溶液的pH专题
分析:25℃时,当溶液的pH=7时,呈中性;当溶液的pH<7时,呈酸性,且pH越小,酸性越强;当溶液的pH>7时,呈碱性,且溶液的pH越大,碱性越强;先将各选项中的量转化成氢氧根离子的浓度,然后找出氢氧根离子浓度最大的即可.
解答:
解:A、25℃时,pH=11的溶液中氢氧根离子浓度为:c(OH-)=
mol/L=1×10-3mol/L;
B、c(OH-)=0.01 mol/L的溶液;
C、氢氧化钠溶液的浓度为:
=0.1mol/L,氢氧化钠为强电解质,则c(OH-)=0.1mol/L;
D、c(H+)=1×10-10mol/L的溶液,则溶液中氢氧根离子浓度为:c(OH-)=
mol/L=1×10-4mol/L;
根据以上分析可知,氢氧根离子浓度最大的是C,则溶液中碱性最强的是C,
故选C.
| 1×10-14 |
| 1×10-11 |
B、c(OH-)=0.01 mol/L的溶液;
C、氢氧化钠溶液的浓度为:
| ||
| 1L |
D、c(H+)=1×10-10mol/L的溶液,则溶液中氢氧根离子浓度为:c(OH-)=
| 1×10-14 |
| 1×10-10 |
根据以上分析可知,氢氧根离子浓度最大的是C,则溶液中碱性最强的是C,
故选C.
点评:本题考查了溶液中碱性强弱的判断,题目难度不大,注意掌握溶液的酸碱性与溶液pH之间的关系,明确氢氧根离子浓度越大,则溶液的碱性越强是解答本题的关键.

练习册系列答案
相关题目
下列实验目的可以实现或操作正确的是( )
| A、用托盘天平称取3.23gNaCl固体 |
| B、用10mL量筒量取7.50mL稀盐酸 |
| C、分液以后下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| D、稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
下列化学用语错误的是( )
A、过氧化钡的电子式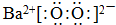 | ||
B、钠-23的原子符号
| ||
| C、次氯酸的结构式 H-Cl-O | ||
| D、锰酸根MnO42- |
实验室将NaClO3和Na2SO3按物质的量之比1:2倒入烧瓶中,用水浴加热,同时滴入H2SO4,产生气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为( )
| A、Cl2 |
| B、Cl2O |
| C、ClO2 |
| D、Cl2O3 |
下列说法正确的是( )
| A、摩尔是物质的质量单位 |
| B、物质的量是国际单位制中七个基本单位之一 |
| C、阿伏加德罗常数是12 g 12C中含有的碳原子数目 |
| D、标准状况下,1 mol H2O所占的体积为22.4L |
下列物质按照酸、碱、盐、氧化物的顺序排列的是( )
| A、盐酸、纯碱、硫酸亚铁、生石灰 |
| B、硫酸、熟石灰、硝酸钾、五氧化二磷 |
| C、氢硫酸、消石灰、干冰、硫酸铜 |
| D、硝酸、苛性纳、碱式碳酸铜、熟石灰 |
分类是重要的科学研究方法,下列物质归类不正确的是( )
| A、电解质:明矾、冰醋酸、硫酸钡 |
| B、酸性氧化物:CO2、SO2、NO、SiO2 |
| C、混合物:铝热剂、矿泉水、水玻璃、漂白粉 |
| D、同素异形体:C60、C70、金刚石 |
富含维生素A的食物为( )
| A、动物肝脏 | B、水果 |
| C、谷物 | D、面包 |
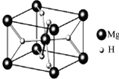 MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为
MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为