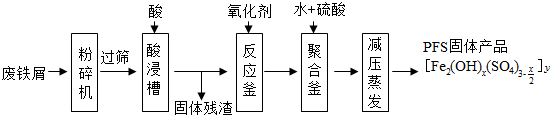
��Ŀ����
5�������й���������ȷ���ǣ�������| A�� | CH4��P4�ķ��ӽṹ�������������Σ������6.02��1023��CH4���ӻ�P4�����ж�����4��6.02��1023�����ۼ� | |
| B�� | �ں�6.02��1023����ԭ�ӵĶ������辧���к���4��6.02��1023��Si-O�� | |
| C�� | 28g CO��C2H4�������ķ�������NA�����ԼΪ22.4L | |
| D�� | 6.02��1023��Fe3+��ȫˮ����Եõ�6.02��1023������������������ |
���� A�������к�4��C-H�����������к�6��p-p����
B����6.02��1023����ԭ�ӵĶ������辧������ʵ���Ϊ1mol����1mol���������к�4molSi-O����
C��û��ָ����������ܼ��㣻
D��һ���������������Ƕ�����������ľۼ��壮
��� �⣺A�����麬4��C-H����������6��p-p������6.02��1023��CH4�����к�4molC-H������4NA����6.02��1023��P4�����к�6molp-p������6NA������A����
B��1mol�������躬1mol��ԭ�ӣ��ʺ�6.02��1023����ԭ�ӵĶ������辧������ʵ���Ϊ1mol����1mol���������к�4molSi-O������4NA������B��ȷ��
C��28g CO��C2H4�������ķ�������NA������û��ָ������£������ù�ʽ���㣬��C����
D��һ���������������Ƕ�����������ľۼ��壬�ʵõ���������������С��NA������D����
��ѡB��
���� ���⿼���˰���٤���������йؼ��㣬�������չ�ʽ��ʹ�ú����ʵĽṹ�ǽ���ؼ����ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
15����ҵ���ö��Ե缫���NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ������˵����ȷ���ǣ�������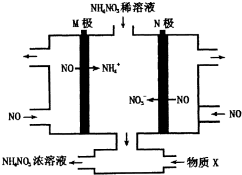

| A�� | M������ֱ����Դ������ | |
| B�� | �����ϵĵ缫��ӦΪ��NO-3e-+4OH-=NO3-+2H2O | |
| C�� | Ϊʹ������ȫ��ת��ΪNH4NO3Ũ��Һ���貹�������X����XΪNH3 | |
| D�� | װ���м���ϡNH4NO3��Һ��Ŀ����Ϊ�������Һ�ĵ�������������NaNO3��Һ���� |
16������������Ԫ��X��Y��Z��Ԫ�����ڱ��е����λ����ͼ��ʾ������˵��һ����ȷ���ǣ�������


| A�� | ��������ϼۣ�Z��X | |
| B�� | X��Y��Z�ĵ����У�Z���ʵ��۵���� | |
| C�� | ��XΪ�ǽ���Ԫ�أ������Ӱ뾶��Xn-��Ym-��Zm- | |
| D�� | X����������Ӧ��ˮ���Ҫô��ǿ�ᣬҪô��ǿ�� |
13����ѧ������������������ɳ�����չ������أ�����˵����ȷ���ǣ�������
| A�� | ����ʹ��̫���ܡ����ܵȜ[����Դ�ܼ���PM2.5����Ⱦ | |
| B�� | �ú��г�ɫ����K2Cr207����������Ƽݣ��������Ҵ��Ļӷ��Ժ������� | |
| C�� | ��ʳ��Ƶ�����ԭ��Ϊ����ˮ���������ǣ���������ˮ��õ��ƾ� | |
| D�� | ��ͭ��ˮ��ͷ���Ӵ��ĸ���ˮ���������ⸯʴ |
20��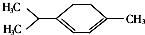 �������ǿ�ű��Чҩ������������ͼ��ʾ�л���Ҳ�������������ڸ��л�����й�˵����ȷ���ǣ�������
�������ǿ�ű��Чҩ������������ͼ��ʾ�л���Ҳ�������������ڸ��л�����й�˵����ȷ���ǣ�������
 �������ǿ�ű��Чҩ������������ͼ��ʾ�л���Ҳ�������������ڸ��л�����й�˵����ȷ���ǣ�������
�������ǿ�ű��Чҩ������������ͼ��ʾ�л���Ҳ�������������ڸ��л�����й�˵����ȷ���ǣ�������| A�� | ���л����һ��ȡ�����У����������칹��8�� | |
| B�� | ���л���λ��ͬһƽ���ڵ�̼ԭ�������10�� | |
| C�� | ���л���������ˮ���ɷ����ӳɡ������;ۺϷ�Ӧ | |
| D�� | ���л�������ʽΪC5H8����ױ���Ϊͬϵ�� |
10�������й��л����˵����ȷ���ǣ�������
| A�� | C8H10����������ͬ���칹����3�� | |
| B�� | ��ϩ�ᣨCH2=CHCOOH����ɽ���ᣨCH3CH=CHCH=CHCOOH����ͬϵ�� | |
| C�� | ��֬��һ��������ˮ��ɸ�֬������ͣ���Ϊ������Ӧ | |
| D�� | �������ǿ�ű����Чҩ���ṹ��ͼ��ʾ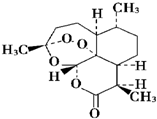 �������������������Ѽ���������ˮ���������ȷ¡���ͪ�ȣ����������Ѵ�ֲ������ȡ���ܹ�����ˮ�ⷴӦ������ǿ������ �������������������Ѽ���������ˮ���������ȷ¡���ͪ�ȣ����������Ѵ�ֲ������ȡ���ܹ�����ˮ�ⷴӦ������ǿ������ |
17����FeSO4��Һ�м��루NH4��2SO4������Ʊ���������茶���[��NH4��2S4•FeSO4•6H2O]���þ����һ���������ȶ������ױ�������������ˮ���������Ҵ���
��1������FeSO4��Һʱ��Ҫ��������ϡ�����Ŀ��������FeSO4��ˮ�⣬�ж�FeSO4��Һ�Ƿ���ʵķ�����ȡ����FeSO4��Һ���Թ��У�����Һ�м���KSCN��Һ������Һ��죬��˵��FeSO4��Һ���ʣ����������ʣ�
��2��ʵ����ͨ����FeSO4��Һ�м��뱥�ͣ�NH4��2SO4��Һ��Ȼ����һϵ�в�������õ���������茶��壬���С�һϵ�в���������Ϊ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��3��Ϊ��ϴ����������茶���Ĵֲ�Ʒ�����з���������ʵ���d������ĸ����
a������ˮϴ b��������ˮϴ��������ˮ�Ҵ�ϴ
c����Na2SO4��Һϴ d������ˮ�Ҵ�ϴ
��4��Ϊ�˲ⶨ�������������Ʒ�Ĵ��ȣ���ȡag��Ʒ����ˮ�����Ƴ�500mL��Һ��ȡ����Һ25.00mL
��Ũ��Ϊcmol•L-1������KMnO4��Һ�ζ����ظ���������2�Σ�ʵ�������£�
�ٵζ������з�����Ӧ�����ӷ���ʽΪMnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
�ڵζ��յ�����������һ�ε��룬��Һ����ɫ��Ϊdz��ɫ����30s����ɫ����
�۸ò�Ʒ�Ĵ���Ϊ$\frac{980c}{a}$��100%���ú�a��c�Ĵ���ʽ��ʾ����
���ϱ��е�һ��ʵ���¼���������Դ��ں����Σ���ԭ�������bc������ĸ����
a��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ�ʱ���Ը��������Һ�����
b���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������
c����һ�εζ��õ���ƿ�ô�װҺ��ϴ��������������ϴ
d�������Ը�����ر�Һδ�������ữ�����������ữ��
��1������FeSO4��Һʱ��Ҫ��������ϡ�����Ŀ��������FeSO4��ˮ�⣬�ж�FeSO4��Һ�Ƿ���ʵķ�����ȡ����FeSO4��Һ���Թ��У�����Һ�м���KSCN��Һ������Һ��죬��˵��FeSO4��Һ���ʣ����������ʣ�
��2��ʵ����ͨ����FeSO4��Һ�м��뱥�ͣ�NH4��2SO4��Һ��Ȼ����һϵ�в�������õ���������茶��壬���С�һϵ�в���������Ϊ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��3��Ϊ��ϴ����������茶���Ĵֲ�Ʒ�����з���������ʵ���d������ĸ����
a������ˮϴ b��������ˮϴ��������ˮ�Ҵ�ϴ
c����Na2SO4��Һϴ d������ˮ�Ҵ�ϴ
��4��Ϊ�˲ⶨ�������������Ʒ�Ĵ��ȣ���ȡag��Ʒ����ˮ�����Ƴ�500mL��Һ��ȡ����Һ25.00mL
��Ũ��Ϊcmol•L-1������KMnO4��Һ�ζ����ظ���������2�Σ�ʵ�������£�
| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ���ĸ��������Һ�����/ml | 25.52 | 25.02 | 24.98 |
�ڵζ��յ�����������һ�ε��룬��Һ����ɫ��Ϊdz��ɫ����30s����ɫ����
�۸ò�Ʒ�Ĵ���Ϊ$\frac{980c}{a}$��100%���ú�a��c�Ĵ���ʽ��ʾ����
���ϱ��е�һ��ʵ���¼���������Դ��ں����Σ���ԭ�������bc������ĸ����
a��ʵ�����ʱ���ӿ̶��߶�ȡ�ζ��յ�ʱ���Ը��������Һ�����
b���ζ�ǰ�ζ��ܼ��������ݣ��ζ�����������
c����һ�εζ��õ���ƿ�ô�װҺ��ϴ��������������ϴ
d�������Ը�����ر�Һδ�������ữ�����������ữ��
14��������ʵ�п�������������ԭ��˵�����ǣ�������
| A�� | HCl������ˮ | B�� | I2������ˮ | C�� | Cl2������ˮ | D�� | CO2������ˮ |