题目内容
15.燃烧法是测定有机物化学式的一种重要方法.现在完全燃烧0.1mol某烃,将燃烧产物CO2和H2O依次通过足量的浓硫酸和浓氢氧化钠溶液,实验结束后,称得浓硫酸增重12.6g,浓氢氧化钠溶液增重26.4g.求:(1)该有机物的分子式;
(2)该有机物可能的结构简式.
分析 根据浓硫酸具有吸水性,增重10.8g,为水的质量,可求得烃中H原子个数,生成物通入碱溶液,增重的质量为二氧化碳的质量,可求得烃中C原子个数,以此可求得烃的分子式,根据计算结果结合同分异构体的书写原则写出其可能结构.
解答 解:(1)浓硫酸增重的12.6g为水的质量,则n(H2O)=$\frac{12.6g}{18g/mol}$=0.7mol,n(H)=2n(H2O)=2×0.2mol=1.4mol,即0.1mol烃中含有1.4molH原子,该烃分子中H原子个数=$\frac{1.4mol}{0.1mol}$=14,
浓氢氧化钠溶液增重的26.4g为二氧化碳的质量,则n(CO2)=$\frac{26.4g}{44g/mol}$=0.6mol,n(C)=n(CO2)=0.6mol,即0.1mol烃中含有0.6molC原子,该烃分子中C原子个数=$\frac{0.6mol}{0.1mol}$=6,
所以该烃的分子式为C6H14,
答:该烃的分子式为C6H14;
(2)该烃的分子式为C6H14,为己烷,
主链为6个碳原子时:CH3CH2CH2CH2CH2CH3;
主链为5个碳原子时:(CH3)2CHCH2CH2CH3、CH3CH2CH(CH3)CH2CH3;
主链为4个碳原子时:(CH3)2CHCH(CH3)2、(CH3)3CCH2CH3 ,
答:该烃的同分异构体的有:CH3CH2CH2CH2CH2CH3、(CH3)2CHCH2CH2CH3、CH3CH2CH(CH3)CH2CH3、(CH3)2CHCH(CH3)2、(CH3)3CCH2CH3 .
点评 本题考查有机物分子式、结构简式的确定,题目难度不大,侧重于学生的分析、计算能力的考查,根据原子守恒法来解答,注意掌握同分异构体的书写原则.

 小学期末标准试卷系列答案
小学期末标准试卷系列答案| A. | CH3CH(OH)CH2COOH系统命名法命名3-羟基丁酸 | |
| B. | 四苯基乙烯(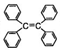 )中所有碳原子一定处于同一平面 )中所有碳原子一定处于同一平面 | |
| C. | lmol 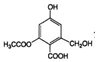 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol | |
| D. | 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应 |
(1)NaCN的电子式为Na+
 .
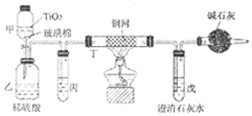
.(2)甲中反应的化学方程式为NaCN+NaClO=NaCNO+NaCl,乙中反应的离子方程式为2CNO-+2H++3ClO-=N2↑+2CO2↑+3Cl-+H2O、2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O.
(3)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,丙中加入饱和食盐水,则装置的作用为除去氯气中的氯化氢.
(4)设计一个确定CN-被处理的百分率的实验方案过滤、洗涤、干燥、称量戊中沉淀的质量,计算出CN-被处理的百分率,装有碱石灰的干燥管的作用是防止空气中的二氧化碳进入戊装置影响沉淀测定的准确度.
(5)氢氰酸(HCN)是现代最早广泛使用的熏蒸之一,可以用于防治各种仓储害虫.在含有NaCN的废液中通入CO2可以制备氢氰酸.己知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |

| A. | a电极是该电池的负极,发生氧化反应 | |
| B. | b电极反应式为2NO3-+10e-+12H+═N2↑+6H2O | |
| C. | 电池工作时,H+由左室通过质子交换膜进入右室 | |
| D. | 转化室中发生反应后溶液的pH增大(忽略体积变化) |
| A. | 碘水 | B. | 氯化钠溶液 | C. | 氢氧化钠溶液 | D. | 溴水 |
| A. | 按系统命名法,化合物 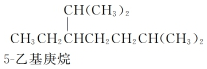 的名称为2,6二甲基5乙基庚烷 的名称为2,6二甲基5乙基庚烷 | |
| B. | 丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 | |
| C. | 化合物  是苯的同系物 是苯的同系物 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
| A. | 是离子化合物,含有离子键和共价键 | |
| B. | 电子式是: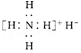 | |
| C. | 与水反应时,氢化铵被氧化 | |
| D. | 固体投入少量的水中,有两种气体产生 |