题目内容
17.下列关于硝酸参加反应的化学方程式或离子方程式书写正确的是( )| A. | 常温下,将铁片置于浓硝酸中:Fe+6HNO3═Fe(NO3)3+3NO2↑+3H2O | |
| B. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向硝酸亚铁溶液中加入稀盐酸:3Fe2++2H++$NO_3^-$═3Fe3++NO↑+H2O | |
| D. | 向浓硝酸中加入铜片:Cu+4H++2$NO_3^-$═Cu2++2NO2↑+2H2O |
分析 A.常温下,浓硝酸能够使铁钝化;
B.硝酸具有强氧化性,能够将Fe2+氧化成Fe3+;
C.二价铁离子被硝酸根氧化生成三价铁离子,硝酸根被还原为NO,该方程式电荷不守恒且氧原子也不守恒;
D.铜片加入浓硝酸中,反应生成Cu2+、NO2和H2O.
解答 解:A.常温下,浓硝酸能够使铁表面形成一层致密的氧化物薄膜,发生钝化,不能持续反应生成Fe(NO3)3,故A错误;
B.Fe3O4与稀硝酸反应的离子反应为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故B错误;
C.向硝酸亚铁溶液中滴加盐酸,离子方程式:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,故C错误;
D.铜片加入浓硝酸中,反应生成Cu2+、NO2和H2O,反应的离子方程式为Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重硝酸有关的离子反应及氧化还原反应的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | |
| B. | 标准状况下,11.2 LSO3含有的分子数目为0.5 NA | |
| C. | 7.8gNa2O2所含的离子数为0.4NA | |
| D. | 11.2LCl2完全溶于NaOH溶液,电子转移数为0.5 NA |
12.工业上利用反应在3Cl2+2NH3═N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应Cl2被氧化 | ||
| C. | 该反应不属于复分解反应 | D. | 生成1mol N2有6mol电子转移 |
2.下列属于物理变化的是( )
| A. | 粮食酿酒 | B. | 食物变质 | C. | 冰雪消融 | D. | 石油裂解 |
9.已知在1×105 Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
| A. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=+242 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ/mol | ||
| C. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+242 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol |
6.常温下,在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | |
| B. | 常温下pH=12的溶液:Na+、K+、SiO32-、NO3- | |
| C. | c(Fe3+)=0.1mol•L-1的溶液:H+、Al3+、I-、SCN- | |
| D. | 加入铝粉生成H2的溶液:K+、Mg2+、SO42-、HCO3- |
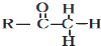 +
+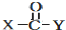 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$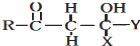
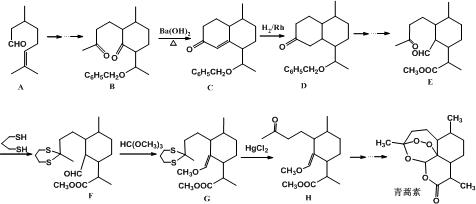
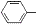 CH2CH2CHO)的路线流程图.路线流程图示例如下:
CH2CH2CHO)的路线流程图.路线流程图示例如下: .
.