题目内容
下列叙述中错误的是( )
| A、原子半径:Cl>S>O |
| B、还原性:Na>Mg>Al |
| C、稳定性:HF>HCl>HBr |
| D、酸性:HClO4>H2SO4>H3PO4 |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断;
B.同周期元素从左到由元素的金属性逐渐减弱.
C.元素的非金属越强,对应的氢化物越稳定;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
B.同周期元素从左到由元素的金属性逐渐减弱.
C.元素的非金属越强,对应的氢化物越稳定;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
解答:
解:A.同周期元素从左到右原子半径逐渐减小,同主族元素从上到下逐渐增大,故原子半径:S>Cl>O,故A错误;
B.同周期元素从左到由元素的金属性逐渐减弱,金属性越强,对应的单质的还原性越强,则还原性:Na>Mg>Al,故B正确;
C.非金属性F>Cl>Br,元素的非金属越强,对应的氢化物越稳定,故C正确;
D.非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故D正确.
故选A.
B.同周期元素从左到由元素的金属性逐渐减弱,金属性越强,对应的单质的还原性越强,则还原性:Na>Mg>Al,故B正确;
C.非金属性F>Cl>Br,元素的非金属越强,对应的氢化物越稳定,故C正确;
D.非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故D正确.
故选A.
点评:本题考查元素周期律知识,为高考常见题型,侧重于学生的基础知识的考查,难度不大,注意把握元素周期律的递变规律的主要内容.

练习册系列答案
相关题目
将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是( )
| A、密闭容器中氨气的浓度不变 |
| B、密闭容器中总压强不变 |
| C、密闭容器中混合气体的密度不变 |
| D、2v(NH3)=v(CO2) |
下列离子方程式中不正确的是( )
| A、铝溶于NaOH溶液:Al+2 OH-=Al O2-+H2↑ | ||||
B、实验室内制氯气:MnO2+4H++2Cl-
| ||||
C、碳酸铵溶液与烧碱溶液共热:NH4++OH-
| ||||
| D、氢氧化钙溶液中加入等物质的量的NaHCO3:Ca2++HCO3-+OH-=CaCO3↓+H2O |
日常生活中,常用到化学知识.下列说法不正确的是( )
| A、向煤燃料中加入生石灰,可以减少对大气的污染 |
| B、维生素C高温时容易被破坏,所以不宜热锅爆炒蔬菜 |
| C、可用燃烧的方法鉴别真丝围巾和合成纤维围巾 |
| D、氟利昂(CCl2F2)可以破坏臭氧层,从而导致温室效应 |
下列物质中不属于油脂的是( )
| A、花生油 | B、汽油 |
| C、菜籽油 | D、酥油 |
下列说法中正确的是( )
| A、纯净的电解质在固态时全部属于离子晶体 |
| B、CCl4、CS2及BF3三种分子中所有原子都满足最外层8电子稳定结构 |
| C、用道尔顿的原子结构理论无法解释同位素现象 |
| D、化学键相同,则晶体类型也相同 |
在蒸发皿中加热蒸干并灼烧下列物质的溶液可以得到该物质的固体是( )
| A、Na2SO4 |
| B、NH4HCO3 |
| C、FeCl3 |
| D、Ca(HCO3)2 |
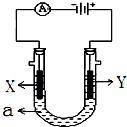 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: