题目内容
17.除去乙酸乙酯中乙酸最好的方法是( )| A. | 用饱和碳酸钠溶液洗 | B. | 用盐酸洗 | ||
| C. | 用氢氧化钠溶液洗 | D. | 用水洗 |
分析 乙酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层,然后分液可除杂,以此来解答.
解答 解:A.酸与饱和碳酸钠溶液反应后,与乙酸乙酯分层,然后分液可除杂,故A正确;
B.乙酸乙酯在酸性条件下可发生水解,故B错误;
C.二者均与NaOH反应,不能除杂,故C错误;
D.水洗除杂不彻底,不能除杂,故D错误;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
8.某原电池构造如图所示,下列说法不正确的是( )


| A. | 负极反应为:Cu-2e-═Cu2+ | |
| B. | 若该原电池工作前两电极质量相等,则工作后,当铜的质量减少6.4g时,两电极质量相差21.6g(假设电解质溶液都是足量的) | |
| C. | 当铜的质量减小12.8 g时,外电路中通过0.4mol电子 | |
| D. | 原电池的总反应式为:Cu+2AgNO3═2Ag+Cu(NO3)2 |
17.某元素原子的核外有四个能层,最外能层有1个电子,该原子核内的质子数不可能为( )
| A. | 19 | B. | 24 | C. | 28 | D. | 29 |
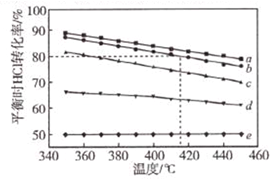 文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图.
文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图. 下列给出了烃及烃的衍生物A、B、C、D、E的相关信息:
下列给出了烃及烃的衍生物A、B、C、D、E的相关信息: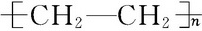 .
.