题目内容
10.在同温同压下,质量相等的氧气和臭氧,它们的分子个数比为3:2,原子个数比为1:1.分析 根据n=$\frac{m}{M}$可知,等质量的氧气和臭氧的物质的量与摩尔质量成反比;根据N=nNA可知,分子数与物质的量成正比;质量相同的氧气和臭氧含有相同的原子数.
解答 解:相等质量的氧气和臭氧,它们的物质的量之比与摩尔质量成反比,则二者的物质的量之比=48g/mol:32g/mol=3:2;
根据N=nNA可知,分子个数之比与物质的量成正比,则二者分子数之比=3:2;
等质量的臭氧和氧气含有等质量的O原子,则含有氧原子个数相等,原子个数之比为1:1,
故答案为:3:2;1:1.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系为解答关键,试题有利于提高学生的分析能力及化学计算能力.

练习册系列答案
相关题目
20.将固体NH4Br置于密闭容器中,在某温度下,发生反应:①NH4Br(s)?NH3(g)+HBr(g),②2HBr(g)?Br2(g)+H2(g),2min平衡后,测知H2的浓度为2mol•L-1,HBr的浓度为4mol•L-1,则在该温度下①平衡常数K是( )
| A. | 20 mol-2•L-2 | B. | 32 mol-2•L-2 | C. | 25 mol-2•L-2 | D. | 16 mol-2•L-2 |
1.下列叙述不正确的是( )
| A. | 质量相等的O2和O3中所含原子数相等 | |
| B. | 物质的量相等的O2和O3中所含分子数相等 | |
| C. | 物质的量相等的CO和CO2中所含原子数相等 | |
| D. | 物质的量相等的CO和CO2中所含碳原子数相等 |
5.下列各元素的性质或原子结构递变规律错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素的最高正价依次升高 | |
| C. | Li、Na、K的金属性依次减弱 | |
| D. | N、O、F原子半径依次增大 |
15.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 1molCl2与足量的铁反应,转移的电子数为3NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 标准状况下,2.24L已烷含有分子的数目为0.1NA | |
| D. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
2.设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A. | 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA | |
| B. | 相同物质的量的CO与CO2 含有碳原子数相同 | |
| C. | 标准状况下,14 g氮气含有的核外电子数为7NA | |
| D. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
20.下列化学用语或模型正确的是( )
| A. | HCl的电子式: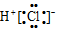 | B. | HClO的结构式:H-Cl-O | ||
| C. | NH4I的电子式: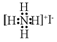 | D. | 甲烷分子球棍模型: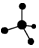 |