题目内容
2.X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同.回答下列问题:
(1)Y和Z的元素名称分别为氧、钠.
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有NaOH、Na2O2.
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是H2O2.
此化合物在酸性条件下与高锰酸钾反应的离子方程式为5H2O2+2MnO4-+6H+═2Mn2++8H2O+5O2↑;
此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为H2O2+CN-+OH-=CO32-+NH3.
分析 短周期元素X、Y和Z的原子序数依次增大.X原子形成的单质是密度最小的气体,则X为H;Y原子的最外层电子数是其周期数的3倍,Y原子只能有2个电子层,最外层电子数为6,则Y为O;Z与X原子最外层电子数相同则Z是钠,据此答题.
解答 解:短周期元素X、Y和Z的原子序数依次增大.X原子形成的单质是密度最小的气体,则X为H;Y原子的最外层电子数是其周期数的3倍,Y原子只能有2个电子层,最外层电子数为6,则Y为O;Z与X原子最外层电子数相同则Z是钠,
(1)根据上面的分析可知,X为氢、Y为氧,Z的元素是钠,故答案为:氧;钠;
(2)由H、O、Na元素组成的化合物中,既含有共价键又含有离子键的有NaOH、Na2O2,故答案为:NaOH;Na2O2;
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质是过氧化氢,过氧化氢在酸性条件下与高锰酸钾反应的离子方程式为5H2O2+2MnO4-+6H+═2Mn2++8H2O+5O2↑,过氧化氢还可将碱性工业废水中的CN-氧化为碳酸盐和氨,方程式为:H2O2+CN-+OH-=CO32-+NH3,
故答案为:H2O2;5H2O2+2MnO4-+6H+═2Mn2++8H2O+5O2↑;H2O2+CN-+OH-=CO32-+NH3.
点评 本题考查了元素位置结构性质的判断,熟悉元素周期表结构是解本题关键,根据原子结构来推断元素,再结合物质的结构、性质来分析解答,题目难度不大.

练习册系列答案
相关题目
13.某元素的一种核素${\;}_{N}^{A}$X,它与2H原子组成HmX分子,在a g HmX中所含中子的物质的量是( )
| A. | $\frac{a}{A}$(A-N)mol | B. | $\frac{a}{A+2m}$ (A-N+m)mol | C. | $\frac{a}{A+2m}$(A-N)mol | D. | $\frac{a}{A+m}$(A-N+m)mol |
10.下列有关物质检验的实验结论正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入用盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| D | 向少量某物质的稀溶液中滴加稀盐酸,产生了能使澄清石灰水变浑浊的气体 | 该物质一定是碳酸盐 |
| A. | A | B. | B | C. | C | D. | D |
14.下列说法不正确的是( )
| A. | 化学反应中一定有化学键断裂,同时也有化学键形成 | |
| B. | 只有共价键的物质一定是共价化合物 | |
| C. | 含有阴离子的化合物一定含有阳离子 | |
| D. | 非金属元素和非金属元素形成的化合物不一定是离子化合物 |
12.下列叙述中能肯定A金属比B金属活泼性强的是( )
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子电子层数比B原子电子层数多 | |
| C. | 1mol A从酸中置换 H+生成的H2比 1mol B从酸中置换H+生成的H2多 | |
| D. | A金属可以把B金属从其盐溶液中置换出来 |
 (PAN)等二次污染物.
(PAN)等二次污染物.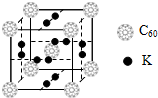 氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.根据要求回答有关问题:
氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.根据要求回答有关问题: