题目内容
1mol锌与足量的稀硫酸反应,求反应后生成的标准状况下的气体的体积为多少升?
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Zn+H2SO4=ZnSO4+H2↑,根据方程式中对比关系计算生成氢气的物质的量,根据V=nVm计算氢气的体积.
解答:
解:令生成氢气的物质的量为n,则:
Zn+H2SO4=ZnSO4+H2↑
1 1
1mol n
n=
=1mol
标况下生成氢气的体积=1mol×22.4L/mol=22.4L
答:标况下生成氢气的体积为22.4L.
Zn+H2SO4=ZnSO4+H2↑
1 1
1mol n
n=
| 1mol×1 |
| 1 |
标况下生成氢气的体积=1mol×22.4L/mol=22.4L
答:标况下生成氢气的体积为22.4L.
点评:本题考查化学方程式的有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
科学家已经合成出氧的一种单质O4,下列关于该物质的说法正确的是( )
| A、摩尔质量是64g |
| B、是氧的一种同位素 |
| C、分子中含有离子键 |
| D、是氧的一种同素异形体 |
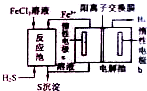 化石燃料开采和加工过程中常有硫化氢废气.工业上可用硫化氢制取氢气,分析化学上硫化氢溶液用作离子分组试剂.
化石燃料开采和加工过程中常有硫化氢废气.工业上可用硫化氢制取氢气,分析化学上硫化氢溶液用作离子分组试剂. 2007年诺贝尔化学奖授予德国科学家格哈德?埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献.
2007年诺贝尔化学奖授予德国科学家格哈德?埃特尔,以表彰他在表面化学研究领域作出的开拓性贡献.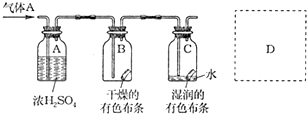
 科学家一直致力于“人工固氮”的方法研究.合成氨的原理为:N2(g)+3H2(g)?2NH3(g),该反应的能量变化如图所示.
科学家一直致力于“人工固氮”的方法研究.合成氨的原理为:N2(g)+3H2(g)?2NH3(g),该反应的能量变化如图所示.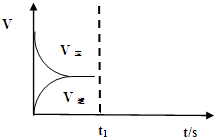 化工工业中常用乙苯脱氢的方法制备苯乙烯.已知某温度下:
化工工业中常用乙苯脱氢的方法制备苯乙烯.已知某温度下: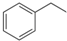 (g)?
(g)?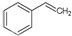 (g)+H2(g),△H=+117.6kJ/mol.
(g)+H2(g),△H=+117.6kJ/mol. (1)双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大.
(1)双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大.