题目内容
根据如下转化关系
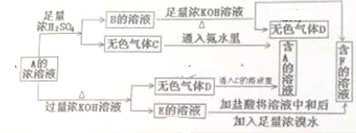
回答下列问题:
(1)物质的分子式:A 、B 、C 、D 、E 、F ;
(2)写出E→F的离子方程式 .

回答下列问题:
(1)物质的分子式:A
(2)写出E→F的离子方程式
考点:无机物的推断
专题:推断题
分析:A的浓溶液与过量浓KOH溶液、加热条件下生成气体D与溶液K,则A含有NH4+,D为NH3,A的浓溶液与足量浓硫酸反应得到气体C与溶液B,A含有弱酸的酸根离子,则B为(NH4)2SO4,F为K2SO4,而K中和后与溴水反应得到K2SO4,故A中含有SO32-或HSO3-,故A为(NH4)2SO3或NH4HSO3,C为SO2,E为K2SO3,据此解答.
解答:
解:(1)A的浓溶液与过量浓KOH溶液、加热条件下生成气体D与溶液K,则A含有NH4+,D为NH3,A的浓溶液与足量浓硫酸反应得到气体C与溶液B,A含有弱酸的酸根离子,则B为(NH4)2SO4,F为K2SO4,而K中和后与溴水反应得到K2SO4,故A中含有SO32-或HSO3-,故A为(NH4)2SO3或NH4HSO3,C为SO2,E为K2SO3,
故答案为:(NH4)2SO3或NH4HSO3;(NH4)2SO4;SO2;NH3;K2SO3;K2SO4;
(2)E→F的离子方程式为:SO32-+Br2+H2O=SO42-+2Br-+2H+,故答案为:SO32-+Br2+H2O=SO42-+2Br-+2H+.
故答案为:(NH4)2SO3或NH4HSO3;(NH4)2SO4;SO2;NH3;K2SO3;K2SO4;
(2)E→F的离子方程式为:SO32-+Br2+H2O=SO42-+2Br-+2H+,故答案为:SO32-+Br2+H2O=SO42-+2Br-+2H+.
点评:本题考查无机物推断,A与酸、碱反应生成气体时推断突破口,再结合转化关系推断,需要学生熟练掌握元素化合物的性质,难度中等.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
某二元弱酸的酸式盐NaHA溶液,若pH<7,则溶液中各粒子的浓度关系不正确的是( )
| A、c(Na+)>c(HA-)>c(H+)>c(A2-)>c(H2A) |
| B、c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-) |
| C、c(H+)+c(A2-)=c(OH-)+c(H2A) |
| D、c(Na+)=c(HA-)+c(H2A)+c(A2-) |
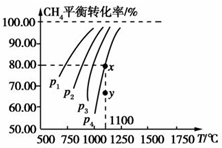 在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )
在2L的恒容密闭容器中,充入0.2molCO2和0.2molCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )| A、上述反应的△H>0 |
| B、压强:P4>P3>P2>P1 |
| C、1100℃,P1时该反应平衡常数约为16.4 |
| D、压强为p4时,在y点:V正>V逆 |
在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)?pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是( )
| A、A的百分含量不再改变 |
| B、各组分的浓度不再改变 |
| C、反应速率υA:υB:υC:υD=m:n:p:q |
| D、单位时间内m mol A断键发生反应,同时p mol C也断键发生反应 |

 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是
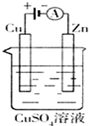
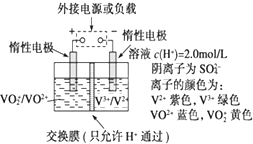 全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示.
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示.