题目内容
6.A、B均为短周期主族元素,其原子的部分电离能(In,单位为kJ•mol-1)数据如表所示:| 序号 | I1 | I2 | I3 | I4 | I5 | I6 | I7 | |
| A的电离能 | 1402 | 2856 | 4578 | 7475 | 9445 | 53267 | … | |
| B的电离能 | 1012 | 1907 | 2914 | 4964 | 6274 | 21267 | 25431 | |
| 序号 | I8 | I9 | I10 | I11 | I12 | I13 | I14 | … |
| B的电离能 | 29872 | 35905 | 40950 | 46261 | 54110 | 59024 | 271791 | … |
分析 同一种元素的原子,其电离能随着失电子个数的增多而增大,当原子失去电子变为稳定状态时,如果继续失电子,则其电离能会出现突变,据此判断该主族元素最外层电子数.
解答 解:已知A、B均为短周期主族元素,由表中数据可知,A、B的电离能I5与I6之间的数据发生突变,即A、B的最外层电子数为5,为第VA族元素,已知A的第一电离能大于B,所以A为N元素,B为P元素,所以A的最高正价为+5价,基态P原子的电子排布式为1s22s22p63s23p3;电负性N大于P,即A的电负性>B的电负性;
故答案为:+5;1s22s22p63s23p3;>.
点评 本题考查了电离能、元素的推断、电负性,第n电离能远远小于第(n+1)电离能时确定原子的最外层电子数,属于基础题,题目难度不大.

练习册系列答案
相关题目
14.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X 的原子半径比Y 的小,X与W 同主族,Z原子的最外层电子数是内层电子数的3倍.下列说法不正确的是( )
| A. | 对应的最简单氢化物的热稳定性:Z>Y | |
| B. | X、Z、W三种元素形成的化合物既含离子键,又含共价键 | |
| C. | 元素X与Y形成的化合物中,每个原子都达到了8电子稳定结构 | |
| D. | X与Z可形成既含极性共价键又含非极性共价键的化合物 |
1.某种溶液仅含下表离子中的5种(不考虑水的电离与离子水解),且各种离子的物质的量均为1mol.
若向原溶液中加入足量的盐酸,有无色气体生成.经分析反应后溶液中阴离子的种类没有变化.
(1)溶液中一定不(填“一定”、“一定不”或“可能”)含有HCO3-或CO32-,理由是HCO3-与CO32-均可与盐酸反应生成二氧化碳,造成阴离子种类有所变化.
(2)原溶液中所含的阴离子为Cl-、NO3-、SO42-,阳离子为Fe2+、Mg2+.
(3)向原溶液中加入足量的盐酸,有无色气体生成的离子反应方程式为3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O.
(4)若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、洗涤、干燥灼烧至恒重,得到固体质量为120g.
| 阳离子 | K+ Ba2+ Fe2+ Al3+ Fe3+ Mg2+ |
| 阴离子 | OH- HCO3- CO32- Cl- NO3- SO42- |
(1)溶液中一定不(填“一定”、“一定不”或“可能”)含有HCO3-或CO32-,理由是HCO3-与CO32-均可与盐酸反应生成二氧化碳,造成阴离子种类有所变化.
(2)原溶液中所含的阴离子为Cl-、NO3-、SO42-,阳离子为Fe2+、Mg2+.
(3)向原溶液中加入足量的盐酸,有无色气体生成的离子反应方程式为3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O.
(4)若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、洗涤、干燥灼烧至恒重,得到固体质量为120g.
11.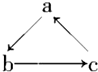 Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
 Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )
Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如表所列物质不能按如图关系(“→”表示一步完成)相互转化的是( )| 选项 | A | B | C | D |
| a | Na | Al | Fe | Cu |
| b | NaOH | Al2O3 | FeCl3 | CuSO4 |
| c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
18.对于反应:M+N-→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高20℃,完成反应的10%需要的时间为( )
| A. | 9 min | B. | 27 min | C. | 13.5 min | D. | 3 min |
15.下列离子方程式正确的是( )
| A. | 锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 稀硝酸和过量的铁粉:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | 少量SO2气体通入NaOH溶液中:SO2+OH-=HSO3- |